在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g) C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
(1)800℃时,0—5min内,以B表示的平均反应速率为
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= ,
该反应为 反应(填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)
惕各酸苯乙酯(C13H16O2)广泛用作香精的调香剂。为了合成该物质,某实验室的科技人员设计了下列合成路线:
试回答下列问题:
(1)A的结构简式为;F的结构简式为。
(2)反应②中另加的试剂是;反应⑤的一般条件是。
(3)反应③的化学方程式为。
(4)上述合成路线中属于取代反应的是(填编号)。
I.下面a~e是中学化学实验中常见的几种定量仪器:
a.量筒 b.容量瓶 c.滴定管 d.托盘天平 e.温度计
①使用容量瓶的第一步操作是___________________________________。
②若用上述仪器配制500mL 2mol·L-1的NaCl溶液,还缺少的玻璃仪器是_________。
③若用上述仪器测定中和热,则缺少的玻璃仪器为烧杯、__________。
④若用上述仪器进行中和滴定,则缺少的仪器是__________。
Ⅱ某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,以探索工业废料的再利用。其实验方案如下: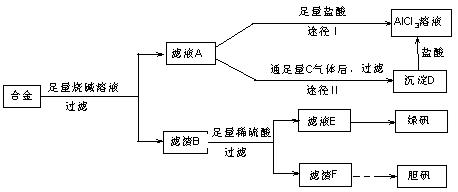
试回答下列问题:
(1)用的器材已有:滤纸、铁架台、铁圈和烧杯,还要补充的玻璃仪器是
。
(2)由滤液A制得AlCl3溶液有途径Ⅰ和Ⅱ两条,你认为合理的是,理由是 。
。
(3)从滤液E中得到绿矾晶体的实验操作是。
(4)写出用滤渣F制备胆矾晶体的有关化学方程式
。
(5)有同学提出可将方案中最初溶解合金的烧碱改用盐酸,重新设计方案,也能制得三种物质,你认为后者的方案是否更合理,理由是
。
某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色:J分子内有两个互为对位的取代基,在一定条件下有如下的转化关系:(无机物略去)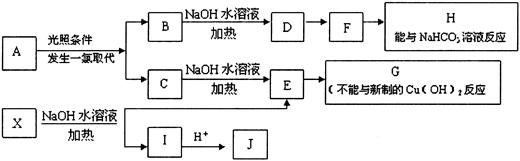
(1)属于芳香烃类的A的同分异构体中,其沸点的大小关系为____________________。(不包括A,用结构简式表示)
(2)J中所含的含氧官能团的名称为____________________。
(3)E与H反应的化学方程式是_______________;反应类型是__________。
(4)B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物M,以M为单体合成的高分子化合物的名称是__________。
(5)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式。
①与FeCl3溶液作用显紫色;②与新制Cu(OH)2悬浊液作用产生红色沉淀;③苯环上的一卤代物有2种。
_______________________________________
在一定条件下,经不同的化学反应,可实现如下图的各种变化。其中只有反应①、②属非氧化还原反应。X、Y为单质,其余为化合物,B是直线型分子,⑤是化学工业上的重要反应。据此请填空: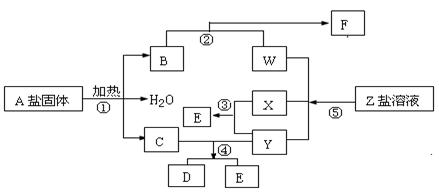
(1)写出下列物质的化学式:
A:X:Y:。
(2)写出反应②的离子方程式:。
(3)1 g X与Y完全反应放热91.5 kJ,反应③的热化学方程式
。
(4)反应④中C与Y的物质的量之比为1:3,D中只含两种元素,则D是。
A、B、C、D四种短周期元素的原子序数依次增大,B的核电荷数是A、D核电荷数之和的2/3;A能分别与B、C、D形成电子总数相等的分子X、 Y、Z。回答下列问题:
Y、Z。回答下列问题:
(1)B、D两元素的名称分别是________、______。
(2)化合物B2A2的电子式为________。
(3)Y与C的最高价氧化物的水化物刚好完全反应时,其生成物的水溶液呈_____性(填“酸”、“碱”或“中”),原因是:(用离子方程式表示)。
(4)在(3)所得生成物的水溶液中,存在如下关系,用离子浓度符号填写:
①c(H+) += c(OH 一) +;
一) +;
②c(H+)=c(OH一) + 。
(5)用X、D2、NaOH溶液和惰性电极可设计一种燃料电池,该燃料电池的
负极反应为:。
正极反应为:。