甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是
| A.反应①中的能量变化如上图所示 |
| B.可推知2H2(g)+O2(g)=2H2O(g)ΔH=-483.8 kJ/mol |
| C.1 mol CH3OH充分燃烧放出的热量为192.9 kJ |
| D.CH3OH转变成H2的过程一定要吸收能量 |
.下列说法正确的是
A.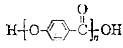 的结构中含有酯基 的结构中含有酯基 |
| B.顺-2-丁烯和反-2-丁烯的加氢产物不同 |
C.1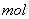 葡萄糖可水解生成2 葡萄糖可水解生成2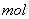 乳酸( 乳酸(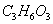 ) ) |
| D.油脂和蛋白质都是能发生水解反应的高分子化合物 |
下列化合物中既易发生取代反应,也可发生加成反应,还能使酸性KMnO4溶液褪色的是
| A.乙烷 | B.乙醇 | C.苯 | D.丙烯 |
下列各组中的反应,属于同一反应类型的是()
| A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 |
| B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 |
| C.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇 |
| D.由氯代环己烷消去制环己烯;由丙烯加溴制1,2-二溴丙烷 |
下列鉴别方法可行的是
| A.用氨水鉴别Al3+、Mg2+和Ag+ |
| B.用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 |
| C.用Ba(NO3)2溶液鉴别Cl-、SO42-和CO32- |
| D.用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO |
下列叙述错误的是
| A.用新制的银氨溶液可区分甲酸甲酯和乙醛 |
| B.用高锰酸钾酸性溶液可区分乙烷和3-乙烯 |
| C.用水可区分苯和溴苯 |
| D.用金属钠可区分乙醇和乙醚 |