金属M和N可构成如图所示的装置.下列分析正确的是 
| A.金属活泼性N>M |
| B.M逐渐溶解 |
| C.负极反应为2H++2e- =H2↑ |
| D.SO42-向M极定向移动 |
混合下列各组物质使之充分反应,将所得混合物加热蒸干,并在300℃灼烧至质量不变为止,最终残留固体为纯净物的是
| A.向CuSO4溶液中加入适量铁粉 | B.等浓度等体积的(NH4)2SO4和BaCl2 |
| C.等物质的量的NaHCO3和Na2O2 | D.在NaBr溶液中通入过量的Cl2 |
下列各选项中对应的实验操作、现象和结论均正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
在试管中滴入适量C2H5X与NaOH溶液,振荡、加热、静置分层后,取水层加稀硝酸酸化,再滴加数滴AgNO3溶液 |
淡黄色沉淀 |
证明卤代烃中含有溴元素 |
| B |
将蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口 |
有大量白烟 |
该无机酸一定为盐酸 |
| C |
在大试管中依次加入适量丁醇、过量乙酸、几滴浓硫酸,混合后塞上带长导管的试管塞,放在石棉网上方空气中加热至120℃左右 |
反应液沸腾,冷却静置,上层油状透明液体有水果香味 |
该油状液体为乙酸丁酯 |
| D |
在简易启普发生器中向石灰石中加入浓醋酸,将产生的气体直接通入苯酚钠溶液中 |
苯酚钠溶液产生浑浊 |
酸性:醋酸>碳酸>苯酚 |
在高温高压的水溶液中,AuS-与Fe2+发生反应沉积出磁铁矿(主要成分Fe3O4)和金矿(含Au),并伴有H2S气体生成。对于该反应的说法一定正确的是
| A.氧化剂和还原剂的物质的量之比2:3 |
| B.AuS-既作氧化剂又作还原剂 |
| C.每生成2.24 L气体,转移电子数为0.1mol |
| D.反应后溶液的pH值降低 |
反应2NO2(g) N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2O4(g) + 57 kJ,若保持气体总质量不变。在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是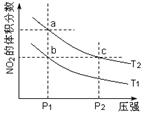
| A.a、c两点气体的颜色:a浅,c深 |
| B.a、c两点气体的平均相对分子质量:a>c |
| C.b、c两点的平衡常数:Kb=Kc |
| D.状态a通过升高温度可变成状态b |
模拟侯氏制碱法原理,在CaCl2浓溶液中通入NH3和CO2可制得纳米级材料,装置见图示。下列说法正确的是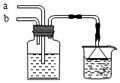
| A.a通入适量的CO2,b通入足量的NH3,纳米材料为Ca(HCO3)2 |
| B.a通入足量的NH3,b通入适量的CO2,纳米材料为Ca(HCO3)2 |
| C.a通入适量的CO2,b通入足量的NH3,纳米材料为CaCO3 |
| D.a通入少量的NH3,b通入足量的CO2,纳米材料为CaCO3 |