(1)肼(N2H4)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,1gN2H4在氧气中完全燃烧生成氮气和H2O,放出19.5kJ热量(25℃时),表示N2H4燃烧热的热化学方程式是____________________________________________________。
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空气燃料电池放电时:正极的电极反应式:__________________;负极的电极反应式:_______________。
(3)下图是一个电解过程示意图。
①锌片上发生的电极反应式是:_____________________________。
②假设使用肼-空气燃料电池作为该过程中的电源,铜片质量变化为128g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积分数为20%)。
聚合物 的合成路线如下:
的合成路线如下:
(1)在合成 的反应路线中:
的反应路线中:
①生成A的反应类型是。
②由B生成 的化学方程式是。
的化学方程式是。
③聚合物 的结构简式是。
的结构简式是。
(2) 的结构简式是。
的结构简式是。
(3)①D的名称是。
②写出生成 的化学方程式。
的化学方程式。
(4)在合成 的反应路线中:
的反应路线中:
①H的分子式是 ,写出
,写出 的化学方程式。
的化学方程式。
②下列说法正确的是。
a. 乙烯与H互为同系物
b. H的同分异构体中存在芳香烃
c. N分子中可能存在碳碳双键
d. H→N的反应原子利用率是100%
工业上常用天然气作为制备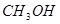 的原料。已知:
的原料。已知:
①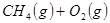
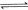
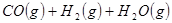
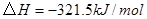
②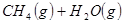
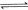
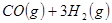
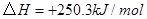
③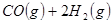
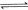
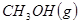
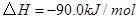
(1)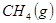 与
与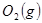 反应生成
反应生成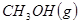 的热化学方程式为。
的热化学方程式为。
(2)向VL恒容密闭容器中充入 与
与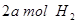 ,在不同压强下合成甲醇。
,在不同压强下合成甲醇。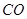 的平衡转化率与温度、压强的关系如下图所示:
的平衡转化率与温度、压强的关系如下图所示: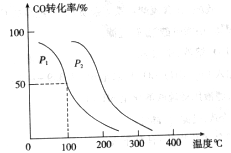
①压强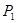
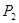 (填“<”、“>”或“=”)
(填“<”、“>”或“=”)
②在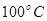 、
、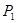 压强时,平衡常数为(用含
压强时,平衡常数为(用含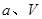 的代数式表示)。
的代数式表示)。
(3)下图是甲醇燃料电池(电解质溶液为稀硫酸)结构示意图,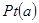 电极通入的
电极通入的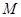 为,电极反应式是。
为,电极反应式是。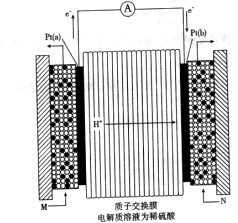
若用该电池电解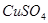 溶液,当得到
溶液,当得到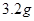 铜时,参加反应的气体
铜时,参加反应的气体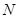 的体积应为
的体积应为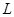 (标准状况)。
(标准状况)。
某同学用工业硫酸铜(含硫酸亚铁等杂质)制备纯净的 。
。
I.取工业硫酸铜固体,用稀硫酸溶解,过滤。
II.向滤液中滴加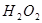 溶液,稍加热。
溶液,稍加热。
III.向II的溶液中加入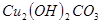 粉末至
粉末至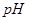 为
为 。
。
IV.加热煮沸,过滤,滤液用稀硫酸酸化至 。
。
V. 加热浓缩、冷却结晶、过滤,得晶体。
已知部分阳离子生成氢氧化物的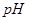 如下表:
如下表:
| 物质 |
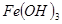 |
 |
 |
开始沉淀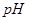 |
2.7 |
7.6 |
4.7 |
完全沉淀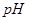 |
3.7 |
9.6 |
6.7 |
(1)II中发生反应的离子方程式是。
(2)II中将 氧化为
氧化为 的目的是。
的目的是。
(3)用 (铁氰化钾)验证II中
(铁氰化钾)验证II中 是否转化完全的现象是。
是否转化完全的现象是。
(4)III中发生反应的离子方程式是。
(5)应用化学平衡移动原理解释IV中“滤液用稀硫酸酸化”的原因。
用 分别滴定
分别滴定 和
和 ,滴定过程中
,滴定过程中 变化曲线如下图所示。
变化曲线如下图所示。
请回答:
(1)滴定盐酸的 变化曲线为(填“图1”或“图2”),判断的理由是
变化曲线为(填“图1”或“图2”),判断的理由是
。
(2)滴定 溶液的过程中,
溶液的过程中,
①当滴加 后,溶液中离子浓度由大到小的顺序为.
后,溶液中离子浓度由大到小的顺序为.
②当 时,溶液
时,溶液 7(填“>”、“=”或“<”)。
7(填“>”、“=”或“<”)。
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。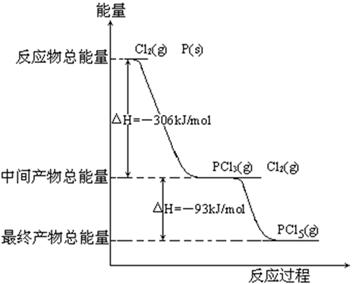
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式_________________________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________________________________,上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,其分解率α1等于_________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2_______α1(填“大于”、“小于”或“等于”)。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是___________________________________。
(4)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
(5)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是_____________________。