下列关于乙酸乙酯实验的说法错误的是
| A.制乙酸乙酯时,向乙醇中缓慢加入浓硫酸和乙酸 |
| B.可将导管插入饱和碳酸钠溶液中收集反应生成的乙酸乙酯 |
| C.1 mol乙醇与2 mol乙酸在浓硫酸催化作用下不能合成1 mol 乙酸乙酯 |
| D.除去乙酸乙酯中含有的乙酸,最好的处理方法是用足量饱和碳酸钠溶液洗涤后分液 |
设某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,且X > 11将上述两溶液分别取等体积充分混合,混合液中各离子的浓度由大到小的顺序是()
A.c(Cl-) c(NH4+) c(NH4+) c(H+) c(H+) c(OH-) c(OH-) |
B.c(NH4+) c(Cl-) c(Cl-) c(H+) c(H+) c(OH-) c(OH-) |
C.c(NH4+) c(Cl-) c(Cl-)  c(OH-) c(OH-) c(H+) c(H+) |
D.c(Cl-) c(NH4+) c(NH4+) c(OH-) c(OH-) c(H+) c(H+) |
可逆反应mA(g)+nB(g) 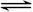 pC(g)+qD(g)的v-t图像如图甲所示,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。
pC(g)+qD(g)的v-t图像如图甲所示,若其他条件都不变,只是在反应前加入合适的催化剂,则其v-t图像如图乙所示。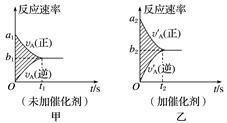
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2⑥t1=t2 ⑦两图中阴影部分
面积相等 ⑧图乙中阴影部分面积更大. 以上所述正确的为( )
| A.②④⑤⑦ | B.②④⑥⑧ | C.②③⑤⑦ | D.②④⑤⑧ |
控制适合的条件,将反应Fe3++Ag Fe2++Ag+ 设计成如图所示的原电池(盐桥装有琼脂—硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后观察到电流计指针向右偏转。下列判断正确的是()
Fe2++Ag+ 设计成如图所示的原电池(盐桥装有琼脂—硝酸钾溶液;灵敏电流计的0刻度居中,左右均有刻度)。已知接通后观察到电流计指针向右偏转。下列判断正确的是()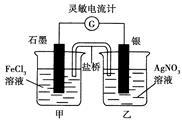
| A.盐桥中的K+移向乙烧杯 |
| B.一段时间后,电流计指针反向偏转,越过0刻度,向左边偏转 |
| C.在外电路中,电子从石墨电极流向银电极 |
| D.电流计指针居中后,往甲烧杯中加入一定量的铁粉,电流计指针将向左偏转 |
将pH=l的盐酸平均分成2份,l份加适量水,另1份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入的水与NaOH溶液的体积比为: ()
| A.9 | B.10 | C.11 | D.12 |
下列有关说法正确的是()
| A.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
B.反应A(g) 2B(g);若正反应的活化能为Ea kJ·mol-1,逆反应的活化能为Eb kJ·mol-1,则该反应的△H =(Ea-Eb)kJ·mol-1。 2B(g);若正反应的活化能为Ea kJ·mol-1,逆反应的活化能为Eb kJ·mol-1,则该反应的△H =(Ea-Eb)kJ·mol-1。 |
C.N2(g)+3H2(g) 2NH3(g) ΔH<0,其他条件不变时升高温度,平衡时氢气转化率增大 2NH3(g) ΔH<0,其他条件不变时升高温度,平衡时氢气转化率增大 |
| D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的ΔS <0 |