A是自然界存在最广泛的ⅡA族元素,常以化合物F存在。从单质A起始发生的一系列化学反应可由下图表示: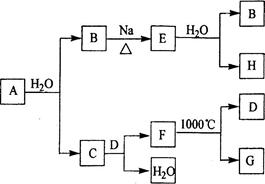
请回答下列问题:
(1)A与水反应的化学方程式为____________,E与水反应的化学方程式为______ _ ______;
(2)F的化学式为_____________,G和D的电子式分别为____________和______________;
(3)D与H反应可能生成的盐有_______ ______ (填化学式);
(4)如何由F制备A : 。
氟卡尼是新型、广谱、高效抗心律失常药,用于多种心律失常的防治。结构为: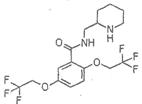 ,它可由龙胆酸(
,它可由龙胆酸(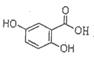 ,为原料合成,合成的方法如下图:
,为原料合成,合成的方法如下图: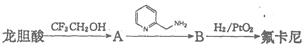
回答以下向题:
(1)写出一种龙胆酸中含有的含氧官能团名称______________;
(2)A的结构简式是____________________________________;
(3)A→B的反应类型是______________;
(4)龙胆酸与甲醇反应生成龙胆酸甲酯,其化学方程式是______________;
(5)满足下列条件的龙胆酸甲酯的同分异构体共有_______种:
①苯环上有3个取代基,其中2个为羟基;②苯环上只有两类氢;③属于酯类。
某有机物A在一定条件下的转化关系如图所示,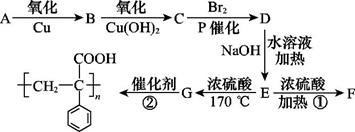
其中两分子E生成环状化合物F,D的结构简式为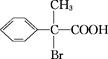
回答下列问题:
(1)写出反应类型:①,②(每空2分)。
(2)写出有机物C、F的结构简式:、(每空2分)。
(3)写出下列化学方程式:A—B:,E—G:(每空2分)。
(4)C的同分异构体有多种,其中属于苯的二取代物,且既能有银镜反应,遇FeCl3溶液又能呈紫色的同分异构体有种,请写出其中任意一种的结构简式:。
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。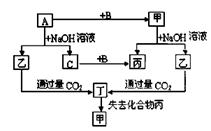
根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A B丁。
(2)元素A在周期表中的位置是,写出甲的一种用 途。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式。
乙与过量CO2反应的离子方程式。
3,4,5-三甲氧基苯甲醛(TMB)是一种药物中间体,以对甲基苯酚为原料的合成路线如下: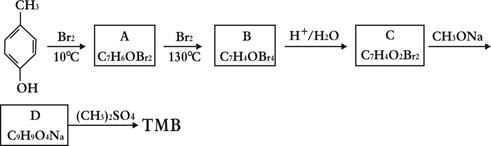
已知:①A(C7H6OBr2)、B(C7H4OBr4)、C(C7H4O2Br2)、D(C9H9O4Na)均有3种不同化学环境的氢;
②C能发生银镜反应;③同一个碳原子连有2个羟基时,易脱水形成醛基。
④3,4,5-三甲氧基苯甲醛(TMB): 请回答下列问题:
请回答下列问题:
(1)TMB的分子式为;A→B的反应类型是反应。
(2)对甲基苯酚的同分异构体中含有苯环的共有种.
(3)对甲基苯酚→A的化学方程式为。
(4)符合下列条件的TMB的同分异构体共有种,写出这些异构中所有能发生银镜反应的结构简式:。
①含有苯环和酯基.
②不含过氧键(-O-O-),且不与FeCl3发生显色反应.
③核磁共振氢谱只出现四组峰.
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E元素是第四周期元素中未成对电子数最多的元素,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,1mol配合物与足量的AgNO3溶液反应能立即生成3molAgCl。F原子的一种核素的质量数为65,中子数为 36。请根据以上情况,回答下列问题:(答题时要用元素符号表示)
(1)B氢化物与HCl反应生成的含有B元素粒子的空间构型是.F元素原子的最外层电子数为个。
(2)B3-离子分别与AC2、由B、C组成的气态化合物互为等电子体,则B、C组成的化合物化学式为;B3-离子还可以和一价阴离子互为等电子体,这阴离子电子式为,这种阴离子常用于检验日常生活中的一种金属阳离子,这金属阳离子符号为
(3)A、B、C的第一电离能由小到大的顺序为
(4)E3+的核外电子排布式是,ECl3形成的六配位的配合物化学式为。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
(6)在F的+1价氧化物的晶胞结构如图,F为 球(“黑”“白”)