某化学兴趣小组采用下列方法测定Na2SO3样品中Na2SO4的质量分数。
【方法一】 测 SO2质量法采用如图所示装置,通过实验测定生成SO2的质量。
测 SO2质量法采用如图所示装置,通过实验测定生成SO2的质量。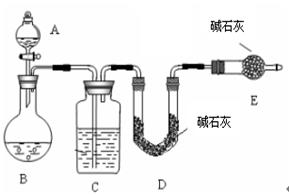
(1)C中盛放的试剂是 ,E装置的作用是 。
(2)若实验前称取m1g样品,再测得SO2的质量为m2g,则可得Na2SO4质量分数,其中m2是通过
测定 (填装置符号)装置在实验前后的质量差得到的。该方法的缺点是(只答一点)
。
【方法二】测沉淀质量法
第一步:称取m3g样品,置于小烧杯中 第二步:向小烧杯中加入足量稀盐酸,加热
第三步:再向小烧杯中加入足量BaCl2溶液,然后过滤、洗涤 第四步:干燥沉淀,称重为m4g
(3)方案中BaCl2能否改成Ba(NO3)2? (填“能”或“不能”); 试简述原因
。
(4)简述洗涤沉淀的方法: 。
(5)若m3=2m4则试样中Na2SO4的质量分数为 。
某学生需要用烧碱固体配制0.5 mol·L-1的NaOH溶液500mL。实验室提供以下仪器:①100mL烧杯②100 mL量筒③1000 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)。请回答下列问题:
(1)计算和称量:需要托盘天平称取NaOH固体g;
(2)实验中必须使用的仪器有_____(填代号),还缺少的仪器是、 。(填仪器名称)
(3)配制时,其正确的操作顺序是(字母表示,每个操作只用一次) ________;
| A.用少量水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡 |
B.在盛有NaOH固体的烧杯中加入适量水 溶解 溶解 |
| C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中 |
| D.将容量瓶盖紧,反复上下颠倒,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
(4)实验两次用到玻璃棒,其作用分别是:先用于________.后用于________;
(5)若出现如下情况,其中将引起所配溶液浓度偏高的是;(填下列编号)
①容量瓶实验前用蒸馏水洗干净,但未烘干②定容观察液面时俯视
③配制过程中遗漏了(3)中步骤A④加蒸馏水时不慎超过了刻度线
(6)若实验过程中出现(5)中④这种情况你将如何处理?。
Ⅰ.对于混合物的分离或提纯,常采用的方法有:①过滤②蒸发结晶③蒸馏④萃取⑤洗气⑥加热分解等。请选用合适的方法序号完成下列填空。
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
(2)除去H2中的CO2,可用的方法除去。
(3)为了从氯化钾和二氧化锰的混合物中获得氯化钾,可先加足量的水溶解,过滤,将得到的滤液
,就可得到氯化钾晶体。
(4)除去氧化钙中的碳酸钙,可用的方法。
(5)从溴水中提取溴单质,可用 方法。
方法。
(6)分离沸点相差较大的液体混合物,可用方法。
Ⅱ.下列仪器常用于物质分离的是__________________(填序号)
①漏斗 ②试管 ③蒸馏烧瓶 ④天平 ⑤分液漏斗 ⑥研钵
二氧化锰(MnO2)与浓盐酸混合加热可得到氯气,下图是制取并探究Cl2化学性质的装置图。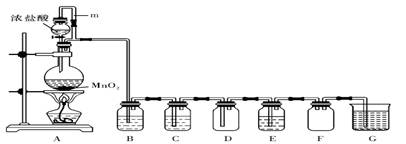
(1)圆底烧瓶中发生反应的化学方程式为 。
(2)A 中m 管的作用是 。
(3)若要得到干燥纯净的气体,则B中应盛放的试剂是。
(4)E中若装有FeCl2 溶液,反应的离子方程式为;
E中若装有淀粉碘化钾溶液,能观察到的实验现象是 。
(5)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象,某中学高一化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体,加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体,加热
c.稀盐酸滴入MnO2 中,然后加入浓硫酸,加热
d.MnO2与NaCl的浓溶液混合,加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是;
实验c的目的是。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是。
下图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器.铁架台.试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
(1)在上述装置中,实验需要加热的仪器按加热的先后顺序排列为(填序号)。
(2)为使A中乙醇平稳地汽化成乙醇蒸气,常用的方法是。
(3)写出B处的现象。
某同学为了验证海带中含有碘,拟进行以下实验,请回答相关问题。
(1)第1步:灼烧。操作时将足量海带灼烧成灰烬,该过程中将使用到的硅酸盐质实验仪器有(填代号,限填3项)
A.试管 B.瓷坩埚 C.坩埚钳 D.三脚架
E.泥三角 F.酒精灯 G.烧杯 H.量筒
(2)第2步:I-溶液的获取。操作是。
(3)第3步:氧化的操作中依次加入合适的试剂。下列氧化剂最好选用(填代号)
A.浓硫酸 B.新制氯水 C.高锰酸钾溶液 D.双氧水
(4)第4步:碘单质的检验,操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含有碘。