某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用,不仅可以提高经济效益,而且还可防止环境污染。现按下列方式进行综合利用: 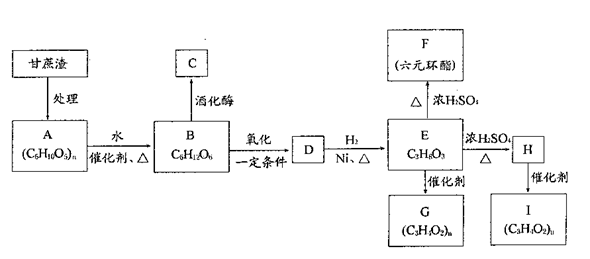
按要求完成问题:
(1)C的官能团名称: ,D的结构简式: ;
(2)写出化学方程式(有机物用结构简式表示):E→F: ,H→I ;
(3)写出下列转化的反应类型:E→G: ,E→H: ;
(4)已知X是B的同分异构体,且满足下列三个条件:
①X为六元环状化合物,含有母体:
②X的母体: 上四个碳原子各连接1个支链或取代基。
上四个碳原子各连接1个支链或取代基。
③l mol X与足量的金属钠反应放出2molH2。
则符合上述条件的X的结构简式共有 种(选填A、B、C、D)。
A.3 B.4 C.5 D.6
选择下列实验方法分离物质,将正确分离方法的序号填在横线上。
A 萃取 B 升华 C 结晶 D 分液 E 蒸馏 F 过滤
(1)分离饱和食盐水与沙子的混合物__________
(2)提取碘水中的碘单质________
(3)分离水和汽油的混合物________
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物________
按要求写出有关氧化还原反应的化学方程式.
(1)是化合反应,也是氧化还原反应_________.
(2)是分解反应,也是氧化还原反应_________.
(3)有金属单质Ag生成的置换反应__________.
(4)不属于四种基本反应类型的氧化还原反应__________.
现有标准状况下的35.5g Cl2,回答下列问题:
(1)其体积约为__________L;
(2)将其与H2在点燃条件完全化合生成HCl,此反应的化学方程式为:__________;
(3)此反应中电子转移的数目约为__________个;
(4)生成的HCl的物质的量为__________mol
(5)将生成的HCl全部溶于水配成溶液,则完全中和这些HCl需要浓度为10mol/L NaOH的体积为__________mL.
有一瓶无色澄清溶液,其中可能含有Na+、Mg2+、Ba2+、Cl-、SO42-、CO32-离子。现进行以下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入NaOH溶液,使溶液由酸性变成碱性,无沉淀产生;
③取少量②中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(1)根据上述事实确定:
该溶液中肯定存在的离子有 ;
肯定不存在的离子有 ;
可能存在的离子有 。
(2)写出③中发生反应的离子方程式 。
(3)检验该溶液中所含的阴离子的试剂是 (填名称)。
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
3.48 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
1.58 |
158 |
| 硝酸银 |
0.02 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于电解质的是__________。
A.蔗糖B.硫酸钾C.高锰酸钾D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 。
(3)配制上述“鲜花保鲜剂” 用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少 , (填写所缺仪器的名称)。
(4)配制溶液时有以下几个操作:
①溶解 ②摇匀 ③洗涤 ④冷却 ⑤称量 ⑥转移溶液 ⑦定容,
正确的操作顺序是 (填序号)。
(5)若定容时俯视容量瓶刻度线,会使所配溶液浓度 (填偏大、偏小、不变)。