I、(1)下列物质中属于强电解质的是 ;(2)属于弱电解质的
是 ;(3)属于非电解质的是 。(填序号)
①氨气 ②氨水 ③盐酸 ④醋酸 ⑤硫酸钡 ⑥银 ⑦氯化钠 ⑧二氧化碳 ⑨醋酸铵 ⑩氢气
II、某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。已知K2S2O8的氧化性比K2Cr2O7强。
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(要求配平)
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 剂。
(3)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 。
某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。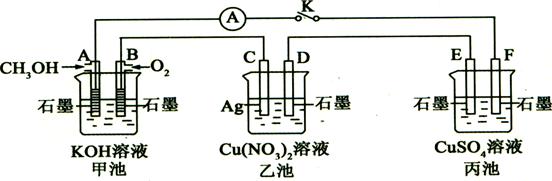
请回答下列问题:
(1)甲池为(填“原电池”、“电解池”或“电镀池”),
A电极的电极反应式为。
(2)丙池中F电极为(填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为。
(3)当乙池中C极质量减轻5.4g时,甲池中B电极理论上消耗O2的体积为ml(标准状况)。
(4)一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是(填选项字母)。
| A.Cu | B.CuO | C.Cu(OH)2 | D.Cu2(0H)2CO3 |
如图A 直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为________极;
(2)滤纸B上发生的总化学方程式为___________________;
(3)欲在电槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为________________,电极f上发生的反应为_____________________,
(4) 槽中放的镀液可以是________或________(只要求填两种电解质溶液)。
已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ 能量,根据图中的能量图,回答下列问题: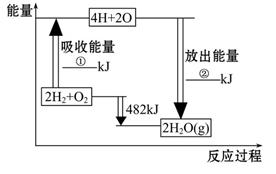
(1)分别写出①②的数值:
①___________KJ;②____________KJ。
(2)生成H2O(g)中的1 mol H—O键放出_____________kJ的能量。
(3)已知:H2O(l)====H2O(g)
ΔH =" +44" kJ·mol-1,试写出2 mol氢气在足量氧气中完全燃烧生成液态水的热化学方程______________________。
发射卫星时可用肼(N2H4)为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
N2(g)+2O2(g) ═2NO2(g)△H1=" +67.7" kJ•mol-1
N2H4(g) +O2(g) ═N2(g)+2H2O(g)△H2=-534 kJ•mol-1
试计算(1)1mol肼和二氧化氮完全反应时放出的热量为 kJ;
(2)写出肼与二氧化氮反应的热化学方程式 。
依据叙述,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g液态甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为______________________。
(2)若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量。其热化学方程式为____________________________________________________________。
(3)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有5NA个电子转移时,放出650kJ的热量。其热化学方程式为____________________。
(4)已知拆开1mol H—H键、1mol N—H键、1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_____________________。