有难溶于水的粉末状固体样品,可能含Al、Fe2O3、Cu2O、SiO2、Fe3O4中的一种或几种。研究小组通过实验确定样品的成分。
查阅资料知:Cu2O + 2H+ =" Cu" + Cu2+ + H2O;
部分氢氧化物在溶液中沉淀的pH见下表:
| 物质 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
| 开始沉淀的pH |
1.8 |
6.3 |
5.2 |
| 完全沉淀的pH |
3.0 |
8.3 |
6.7 |
注:金属离子的起始浓度为0.1 mol·L-1 实验步骤:
Ⅰ.取一定量样品于烧杯中,加足量NaOH溶液,有气体产生,过滤得固体A和无色溶液B;
Ⅱ.向B中加入稀硫酸,出现白色沉淀,继续滴加稀硫酸至过量,白色沉淀完全溶解;
Ⅲ.向A中加入足量稀硫酸并微热,固体完全溶解,得溶液C;
Ⅳ.向C中加入NaClO,调节溶液的pH至4~5,产生红褐色沉淀,过滤得到蓝绿色溶液D;
Ⅴ.向D中加入NaOH,调节溶液的pH到7~8,产生蓝色絮状沉淀。
请回答下列问题。
(1)Ⅰ中产生气体的离子方程式为 。
(2)由Ⅰ、Ⅱ知,原样品中一定不存在的物质是 。
(3)溶液C中除H+、Cu2+外一定还含有另一种阳离子;为验证溶液C中存在该阳离子,可选用的试剂及对应的现象是 。
(4)Ⅳ中加NaClO的目的是 。
(5)将Ⅳ中得到的溶液D电解,若电路中有0.1mol电子通过,则理论上阴极质量增重 g。
(6)由上述实验可以获得结论:原样品所有可能的成分组合为组合1: ;组合2:
;……(用化学式表示)
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。完成下列各题:
(1)正四面体烷的分子式为,其二氯取代产物有种
(2)关于乙烯基乙炔分子的说法错误的是:
a.能使酸性KMnO4溶液褪色
b.1摩尔乙烯基乙炔能与3摩尔Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与苯互为同系物且一氯代物只有两种的物质的结构简式(举两例):
、。
某甲烷和氢气的混合气体共a L,完全燃烧需要的氧气的体积也为a L,则原混合气体中,甲烷和氢气的体积比为______________。
甲烷在氯气中燃烧,可看到集气瓶内壁有黑色固体颗粒生成,瓶口产生大量白雾,根据以上现象分析,上述反应的化学反应方程式为_______________________________。
(一)写出下列有机物的系统命名或结构简式:
(1)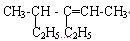 ______________________________
______________________________
(2)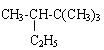
(3)CH3CH(CH3)C(CH3)2(CH2)2CH3
(4)2,5-二甲基-4-乙基庚烷(5) 2-甲基-2-戊烯
__________________________________________ ______________________________________
(二)按要求写出下列化学方程式:(请注明反应条件)
(1)甲苯 →TNT
;
(2)丙烯 → 聚丙烯
;
(3)实验室制备乙烯
;
(4) CaC2→乙炔
。
已知: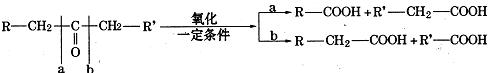
现将A进行如下图所示反应,已知:D的相对分子质量比E小,B不能发生银镜反应,F可使溴水褪色,且其中含甲基。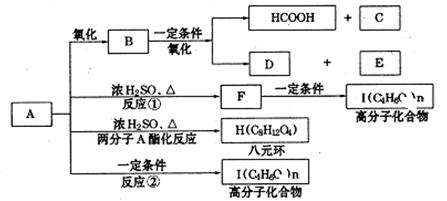
试回答下列问题:
(1)写出下列物质的结构简式:A,C,D;A中所含的官能团名称:。
(2)写出反应①和②的反应类型:反应①,反应②;
(3)写出下列变化的化学方程式:
①F→G:,
②A→H:。