高炉炼铁中发生的基本反应之一如下:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数 。(填“变大”“变小”或“不变”)
(2)1 100 ℃时测得高炉中c(CO2)=0.013 mol·L-1,c(CO)=0.05 mol·L-1,在这种情况下,该反应是否处于化学平衡状态: (填“是”或“否”),此时,化学反应速率是v(正) v(逆)(填“大于”“小于”或“等于”),其原因 。
在试管里放入一块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。
(1)若铜片还有剩余,硫酸________消耗完毕(填“已”或 “没有”)。其理由是___________________________________________________________________。
“没有”)。其理由是___________________________________________________________________。
(2)用一定量的废铜屑制取胆矾,有两种方法:一种是取Cu与浓H2SO4直接反应;二是先将铜在空气中加热使之生成CuO,再与稀H2SO4反应,其中_________种方法好,理由是 _____________________________________________________。
A、B、C、D、E分别为(NH4)2SO4、NH4Cl 、NaCl 、Na2SO4、Ba(OH)2五种溶液中的某一种,把它们两两混合:
(1)A和B混合产生白色沉淀,加热,无明显变化;
(2)B和C混合产生白色沉淀,加热,产生使湿润红色石蕊试纸变蓝的气体;
(3)B和E混合无明显变化,加热,产生使湿润红色石蕊试变蓝的气体。
根据以上现象,判断A、B、C、D、E各为什么物质(写物质名称)。
A:、B:、C:、
D:、E:。
氨气极易溶于水,其水溶液显_________(酸性、中性、碱性)。氨气和氯化氢在空气中相遇时,可以看到的现象是__________。
有一瓶无色气体,可能含有CO2,HCl,HBr,SO2 中的一种或几种气体,将气体通入适量氯水中,得到无色透明的溶液,继续向该溶液中加入少量的BaCl2溶液和盐酸,有白色沉淀产生。则原气体中一定含有__________,肯定不含有__________。
如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质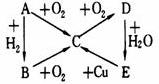
当A是气体单质时,B是______,C是_____,E是______。