已知一个碳原子上同时连有两个羟基时,易发生如下转化: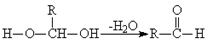
请根据图示回答: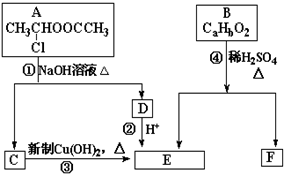
(1)E中含有官能团的名称是_________,③的反应类型是______________,C跟新制的氢氧化铜悬浊液反应的化学方程式为。
(2)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n(H2O) =" 2" :1。F是电脑芯片中高分子光阻剂的主要原料,F具有以下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。则F在一定条件下发生加聚反应的化学方程式为__ ________________________________________________。
(3)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。G可能有种结构,写出其中一种同分异构体的结构简式 ______________。
根据下面各物质之间的转化关系,回答问题: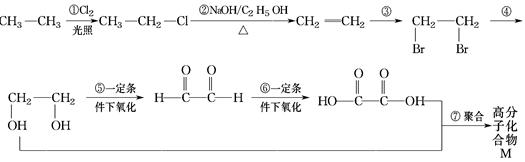
(1)属于取代反应的有(填序号,下同)___________,属于加成反应的有 _________。
(2)写出反应③、④的化学方程式(有机物用结构简式表示,注明反应条件,下同)
a.反应③___________________________________________________________。
b.反应④__________________________________________________________。
(3)写出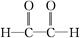 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
___________________________________________________________________。
碳、氢、氧3种元素组成的有机物A,相对分子质量为152,其分子中C、H原子个数比为1∶1,含氧元素的质量分数为31.58%.A遇FeCl3溶液显紫色,其苯环上的一氯取代物有两种,请回答下列问题:(1)A的分子式是____________________.
(2)若A能与NaHCO3溶液反应,A的结构简式为____________________;写出A与NaHCO3溶液反应的化学方程式__________________________________________________________.
(3)如A可以发生如图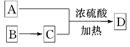 所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式为______________________________________________________。
所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式为______________________________________________________。
(4)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度.甲、乙两装置相比较,乙装置有哪些优点________________________.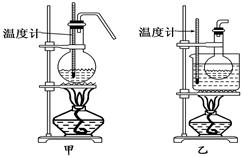
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢原子。
(1)A的结构简式为;
(2)已知A、B、C有下列转化关系,则反应②的化学方程式为;
C的化学名称为。 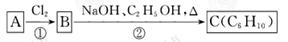
写出下列反应的离子方程式,或相应的化学方程式(每题2分7小题共14分)
(1)石灰石溶于稀盐酸。
(2)稀硫酸与氢氧化钡溶液的反应。
(3)碳酸氢钠溶液与盐酸反应。
(4)氢氧化铜与稀硫酸反应。
(5)2H++ CO32-=CO2↑+H2O 。
(6)Cu+2Ag+=Cu2++2Ag。
(7)CO2+2OH-=CO32-+H2O。