某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1NaOH溶液,实验尚缺少的玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
| 实验用品 |
溶液温度 |
中和热 |
|||
| t1 |
t2 |
ΔH |
|||
| ① |
50 mL 0.55 mol·L-1 NaOH溶液 |
50 mL 0.5 mol·L-1 HCl溶液 |
20 ℃ |
23.3 ℃ |
|
| ② |
50 mL 0.55 mol·L-1 NaOH溶液 |
50 mL 0.5 mol·L-1 HCl溶液 |
20 ℃ |
23.5 ℃ |
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。
①计算完成上表。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。
硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为
和
,还有少量
、
、
、
和
等)为原料制备硼酸(
)的工艺流程如图所示:
回答下列问题:
(1)写出
与硫酸反应的化学方程式。为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有(写出两条)。
(2)利用的磁性,可将其从"浸渣"中分离。"浸渣"中还剩余的物质是(写化学式)。
(3)"净化除杂"需先加
溶液,作用是。然后再调节溶液的
约为5,目的是。
(4)"粗硼酸"中的主要杂质是填名称)。
(5)以硼酸为原料可制得硼氢化钠(
),它是有机合成中的重要还原剂,其电子式为。
(6)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程。
草酸(乙二酸)存在于自然界的植物中,其
=5.4×10-2,
=5.4×10-5。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(
)无色,熔点为101
,易溶于水,受热脱水、升华,170
以上分解。回答下列问题:
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。装置
中可观察到的现象是,由此可知草酸晶体分解的产物中有。装置
的主要作用是。
(2)乙组同学认为草酸晶体分解的产物中含有
,为进行验证,选用甲组实验中的装置
、
和下图所示的部分装置(可以重复选用)进行实验。
①乙组同学的实验装置中,依次连接的合理顺序为
、
、。装置H反应管中盛有的物质是。
②能证明草酸晶体分解产物中有
的现象是。
(3)设计实验证明:
①草酸的酸性比碳酸的强。
②草酸为二元酸。
二氧化氯(
,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:
(1)工业上可用
与
在
存在下制得
,该反应氧化剂与还原剂物质的量之比为。
(2)实验室用
、盐酸、
(亚氯酸钠)为原料,通过以下过程制备
:
①电解时发生反应的化学方程式为。
②溶液
中大量存在的阴离子有。
③除去
中的
可选用的试剂是(填标号)。
a.水 b.碱石灰C.浓硫酸 d.饱和食盐水
(3)用下图装置可以测定混合气中
的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50
水溶解后,再加入3
稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000
硫代硫酸钠标准溶液滴定锥形瓶中的溶液(
),指示剂显示终点时共用去20.00
硫代硫酸钠溶液。在此过程中:
①锥形瓶内
与碘化钾反应的离子方程式为。
②玻璃液封装置的作用是。
③
中加入的指示剂通常为,滴定至终点的现象是。
④测得混合气中
的质量为
。
(4)用
处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是(填标号)。
a.明矾b.碘化钾c.盐酸 d.硫酸亚铁
废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。某化学小组模拟该方法回收铜和制取胆矾,流程简图如下: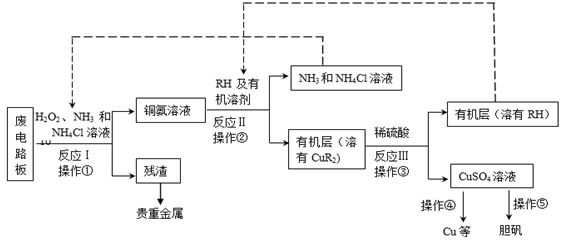
回答下列问题:
(1)反应Ⅰ是将
转化为
,反应中
的作用是。写出操作①的名称:。
(2)反应II是铜氨溶液中的
与有机物RH反应,写出该反应的离子方程式:。操作②用到的主要仪器名称为,其目的是(填序号)。
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加
在水中的溶解度
(3)反应Ⅲ是有机溶液中的
与稀硫酸反应生成
和。若操作③使用下图装置,图中存在的错误是。
(4)操作④以石墨作电极电解
溶液。阴极析出铜,阳极产物是。操作⑤由硫酸铜溶液制胆矾的主要步骤是。
(5)流程中有三次实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是。循环使用的
在反应Ⅰ中的主要作用是。
是常见的化肥和化工原料,受热易分解。某兴趣小组拟探究其分解产物。
[查阅资料]
在260
和400
时分解产物不同。
[实验探究]该小组拟选用下图所示装置进行实验(夹持和加热装置略)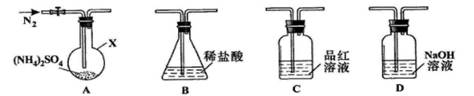
实验1:连接装置
,检查气密性,按图示加入试剂(装置
盛0.5000
盐酸70.00
)。通入
排尽空气后,于260
加热装置
一段时间,停止加热,冷却,停止通入
。品红溶液不褪色,取下装置
,加入指示剂,用0.2000
溶液滴定剩余盐酸,终点时消耗
溶液25.00
。经检验滴定后的溶液中无
。
(1)仪器
的名称是。
(2)滴定前,下列操作的正确顺序是(填字母编号)。
a.盛装0.2000
溶液
b.用0.2000
溶液润洗
c.读数、记录
d.查漏、清洗
e.排尽滴定管尖嘴的气泡并调整液面
(3)装置
内溶液吸收气体的物质的量是
实验2:连接装置
,检查气密性,按图示重新加入试剂。通入
排尽空气后,于400
加热装置
至
完全分解无残留物,停止加热,冷却,停止通入
。观察到装置
、
之间的导气管内有少量白色固体。经检验,该白色固体和装置
内溶液中有
,无
。进一步研究发现,气体产物中无氮氧化物。
(4)检验装置
内溶液中有
,无
的实验操作和现象是.
(5)装置
内溶液吸收的气体是.
(6)
在400
分解的化学方程式是.