二氧化氯(,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:
(1)工业上可用与在存在下制得,该反应氧化剂与还原剂物质的量之比为。
(2)实验室用、盐酸、(亚氯酸钠)为原料,通过以下过程制备:

①电解时发生反应的化学方程式为。
②溶液中大量存在的阴离子有。
③除去中的可选用的试剂是(填标号)。
a.水 b.碱石灰 C.浓硫酸 d.饱和食盐水
(3)用下图装置可以测定混合气中的含量:

Ⅰ.在锥形瓶中加入足量的碘化钾,用50 水溶解后,再加入3 稀硫酸:
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 硫代硫酸钠标准溶液滴定锥形瓶中的溶液(),指示剂显示终点时共用去20.00 硫代硫酸钠溶液。在此过程中:
①锥形瓶内与碘化钾反应的离子方程式为。
②玻璃液封装置的作用是。
③中加入的指示剂通常为,滴定至终点的现象是。
④测得混合气中的质量为。
(4)用处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是(填标号)。
a.明矾 b.碘化钾 c.盐酸 d.硫酸亚铁
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积,并检验氯气。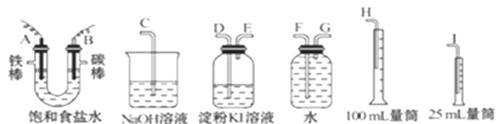
(1)A极发生的电极反应式是______ _______
_______ ______,
______,
B极发生的电极反应式是_______________________。
(2)设计上述气体实验装置时,各接口的正确连接顺序为:
A接______、 _____接______ ;B接_____ 、 _____接______ 。
(3)证明产物中有Cl2的实验现象是______。
(4)已知电解后测得产生的H2的体积为44.8 mL(已经折算成标准状况),电解后溶液的体积为50 mL,此时溶液中NaOH的物质的量浓度为:________。
通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的的质量确定有机物的组成。下图所示的是用燃烧法确定有机物物分子式的常用装置。

回答下列问题:
现准现准确称取0.44 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重0.88 g,B管增重0.36g。请回答:按上述所 给的测量信息,回答问题:
给的测量信息,回答问题:
(1)A、B管内均盛有有固态试剂,A管的作用是______________________;
(2)E中应盛装什么试剂:_______________;
(3)如果把CuO网去掉,A管重量将____;(填“增大”、“减小”、或“不变”)
(4)请改进这套装置的一个不足之处:;
(5)该有 机物的实验式为__________________;
机物的实验式为__________________;
(6)要确定该有机物的分子式,还必须知道的数据是。
甲、乙两同学欲分别完成“钠与氯气反应”的实验。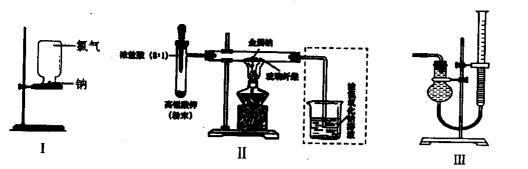
I.甲同学的方案为:取一块绿豆大的金属钠(切去氧化层),用滤纸吸净煤油,放在石棉网上,用酒精灯微热。待钠熔成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方(装置如图I)。该方案的不足之处有(至少答出两点)。
II.乙同学所采用的装置如图Ⅱ,回答下列问题:
(1)按图Ⅱ组装仪器、添加药品,实验开始后,先将浓盐酸挤入试管,试管中发生反应的离子方程式为;待装置中出现现象后,点燃酒精灯。
(2)点燃酒精灯后,玻璃管中出现的现象是。(至少答出三点)
(3)乙同学欲将虚框内装置改为图Ⅲ所示装置,并测量多余气体的体积。
①若图Ⅲ所示量气装置由干燥管、乳胶管和50mL滴定管组装而成,此处所用滴定管是(填“酸式”或“碱式”)滴定管。
②为提高测量的准确性,图Ⅲ装置中的液体可用;收集完气体并冷却至室温后读数,读数前应进行的操作是。
③如果开始读数时操作正确,最后读数时俯视右边滴定管液面,会导致所测气体的体积(填“偏大”、“偏小”或“无影响”)。
中学化学中常见的几种物质存在如下关系,其中甲是黑色非金属单质,乙是生活中常见的金属单质,D是红棕色气体。(图中部分产物和反应条件已略去)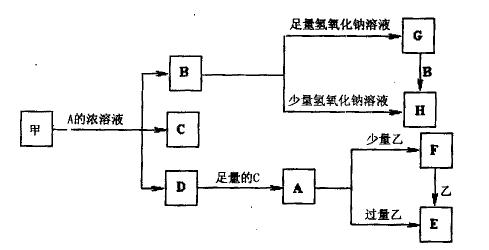
回答下列问题:
(1)写出甲与A的浓溶液反应的化学方程式。
(2)将等体积等浓度的G溶液和H溶液混合后得到的溶液中的离子浓度大小关系为。
(3)除去G固体中含有H杂质采用的方法是。
(4)A溶液与一种能使湿润的红色石蕊试纸变蓝色的气体反应,生成一种盐,该盐的溶液呈酸性,其原因是(用离子方程式表示)。
(5)写出向E溶液中加入少量稀硫酸后反应的离子方程式
。
将溶液F加热蒸干、灼烧到质量不再减少时所得固体物质的化学式为。
(6)确定E中阳离子实验的方法为。
某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如下图所示:
 查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。
查阅资料可知:乙二酸晶体(H2C2O4·2H2O)熔点100.1 ℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu。
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:;
(2)装置B的作用是;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是;。
(3)实验结束后向装置B的试管中加入NaHCO3溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是。
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物。实验小组 进一步探究:
进一步探究:
①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是。
②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L。则红色固体中含单质铜的质量分数是。