已知下列热化学方程式:
①CaCO3(s) CaO(s)+CO2(g) ΔH=+177.7 kJ
CaO(s)+CO2(g) ΔH=+177.7 kJ
②C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
③HCl(l)+NaOH(l) NaCl(l)+H2O(l) ΔH=-57.3 kJ·mol-1
NaCl(l)+H2O(l) ΔH=-57.3 kJ·mol-1
④C(s)+O2(g) CO2(g) ΔH=-393.5 kJ·mol-1
CO2(g) ΔH=-393.5 kJ·mol-1
⑤CO(g)+O2(g) CO2(g) ΔH="-283" kJ·mol-1
CO2(g) ΔH="-283" kJ·mol-1
⑥2H2(g)+O2(g) 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有 。
(2)上述反应中,表示燃烧热的热化学方程式有 。
由原子序数依次增大的五种短周期元素A、B、C、D、E,已知A、E同主族,A元素的原子半径最小,B元素原子的最外层电子数是内层电子数的2倍,C元素最高价氧化物的水化物与其氢化物反应生成一种盐;A、B、C、E四种元素分别都能与D元素形成原子个数比不相同的多种常见化合物,回答下列问题:
(1)B在周期表中的位置是 ,C元素的单质的电子式 。
(2)写出同时含A、B、C、D四种元素的一种盐的化学式 。
(3)E与D形成的一种化合物与BD2发生氧化还原反应,该反应的化学方程式为 。
(4)用A和D两元素组成的单质可以制成一种燃料电池,电池中装有浓KOH溶液。用多孔的惰性电极浸入浓KOH溶液中,两极均有特制的防止气体透过的隔膜,在一极通入A的单质,另一极通入D的单质。则该电池正极的电极反应式为 。
(5)化合物C2A4和C2D4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染。已知1mol C2A4和C2D4完全反应生成两种气体时放出热量516.8KJ,则该反应的热化学方程式为 。
从能量的变化和反应的快慢等角度研究反应: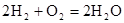 。
。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
| A.使用催化剂 | B.适当提高氧气的浓度 |
| C.适当提高反应的温度 | D.适当降低反应的温度 |
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是________。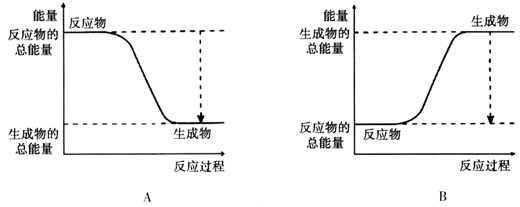
(3)从断键和成键的角度分析上述反应中能量的变化。
【资料】①键能:拆开1mol化学键需要吸收的能量,或是形成1mol化学键所放出的能量称为键能。
②化学键的键能:
| 化学键 |
H—H |
O=O |
H—O |
键能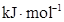 |
436 |
496 |
463 |
请填写下表:
| 化学键 |
填“吸收热量” 或“放出热量” |
能量变化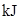 |
|
| 拆开化学键 |
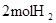 中的化学键 中的化学键 |
_______________ |
_______________ |
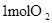 中的化学键 中的化学键 |
|||
| 形成化学键 |
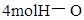 键 键 |
_______________ |
_______________ |
| 总能量变化 |
_______________ |
_______________ |
|
(4)氢氧燃料电池的总反应方程式为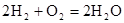 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
A、B、C、D、E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的―1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸。请根据以上信息回答下列问题。
(1)B元素在元素周期表中的位置是 ____________族。
(2)画出D元素的原子结构示意图____________。
(3)与E的氢化物分子所含电子总数相等的分子是_________(举一例、填化学式),离子是____________(举一例、填电子式)。
(4)A与C形成的化合物中含有的化学键的类型是____________。
(5)D的单质与B的最高价氧化物对应的水化物的溶液发生反应的离子方程式是__________________________________________。
氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是: .测量其溶液的pH时,可以 ,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .
(3)用熟石灰来改良酸性土壤,反应的化学方程式是: (以土壤中含有硫酸为例).
(4)用熟石灰粉与草木灰(主要成分是K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.使用时,选择有露水的早晨,把“黑白粉”撒在植物茎叶上,可消除忌碱虫体.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是 (填元素符号).
化学是在原子、分子的水平上研究物质及其变化规律.请回答下列关于水与过氧化氢(H2O2)的问题:
(1)H2O2中氧元素的化合价为 .
(2)1个过氧化氢分子中含有 个H, 个O.
(3)写出下列反应的化学方程式:
①水通电后分解: ;
②过氧化氢分解: .
(4)下列关于它们的说法正确的是 (填编号).
①水、过氧化氢组成元素相同,化学性质也相同
②过氧化氢溶于水得到的物质仍然属于纯净物
③水是生物体内重要的组成物质
④硬水可以使肥皂水产生更多的泡沫.