有下列四种微粒:① 、②
、②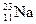 、③
、③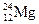 、④
、④ 。用①、②、③、④回答:
。用①、②、③、④回答:
(1)按原子半径由大到小顺序排列的是 ,
(2) 微粒中质子数小于中子数的是 ,
微粒中质子数小于中子数的是 ,
(3)在化合物中呈现的化合价的数值最高的是 ,
(4)能形成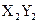 型化合物的是 。
型化合物的是 。
在一容积为2 L的密闭容器内加入0.2 molA和0.6 molB,在一定条件下发生反应:A(s)+3B(g) 2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
2C(s)+3D(g) 已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ |
1000 |
1150 |
1300 |
| 平衡常数 |
64.0 |
50.7 |
42.9 |
请回答下列问题:
⑴该反应的平衡常数表达式K=,ΔH0(填“>”或“<”)。
⑵1000 ℃时,4 min后达到平衡.求4 min内D的平均反应速率v(D)=,B的平衡转化率为,平衡时B的体积分数。
⑶欲提高⑵中B的平衡转化率,可采取的措施是
A.减少C的量B.增加A的量 C.移出部分D
D.降低反应温度 E.减小容器的容积 F.加入合适的催化剂
⑷1000 ℃时, 在一容积为2 L的密闭容器内加入XmolC和0.6 molD,5 min后达到平衡,B的浓度与⑵中B的浓度相同,求X的范围
⑸下列说法中能说明反应已达到平衡状态的是
A.容器内混合气体的压强不随时间变化而变B.B的速率不随时间的变化而变化
C.c(B)︰c(D)=1︰1D.混合气体的密度保持不变(M(B)≠M(D))
常温下,某水溶液中存在的离子有:Na+、B2-、HB-、H+、OH-,存在的分子有H2O、H2B。根据题意回答下列问题:
(1)写出酸H2B的电离方程式﹑。
(2)常温下,已知0.1 mol·L-1二元酸H2B溶液中c(OH-) / c(H+)=1×10-6。
①常温下,0.1 mol·L-1H2B溶液的pH=;
②写出该酸(H2B)与少量NaOH溶液反应的离子方程式:;
(3)常温下,将100 mL 0.1 mol·L-1的稀H2SO4溶液与100 mL 0.4 mol·L-1的NaOH溶液充分混合(溶液体积变化忽略不计),所得溶液的pH=。
(4)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=。该温度下(t℃),0.1 mol·L-1HCl溶液的pH=;
⑴有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融硝酸钾;⑥乙醇; ⑦稀硫酸; ⑧金刚石; ⑨二氧化硫 ; ⑩冰醋酸。
其中能导电的有;属于非电解质的有;属于强电解质的有;(填序号)
⑵常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈性,溶液中c(NH4+)与c(Cl-)的大小关系是:c(NH4+)c(Cl-);
⑶常温下,0.010mol·L-1盐酸和0.010mol·L-1氨水的pH之和14,常温下,pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和14(填>,<或=)
⑷用物质的量浓度为0.04 mol·L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol·L-1的氨水溶液20mL,消耗盐酸12.5mL,则此氨水物质的量浓度为mol·L-1;电离度为。
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是________(用对应的元素符号表示);D原子的基态电子排布式为___________________________________。
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取________杂化;BC的空间构型为________(用文字描述)。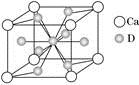 (3)1 mol AB-中含有的π键个数为________。
(3)1 mol AB-中含有的π键个数为________。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比是________。
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=________(填数值);氢在合金中的密度为________。
图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。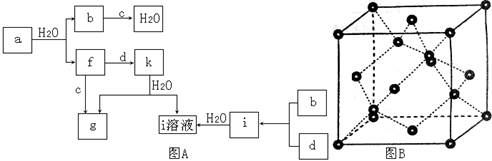
回答下列问题:
(1)图B对应的物质名称是,其晶胞中的原子数为,晶体的类型为。
(2)d中元素的原子核外电子排布式为。
(3)图A中由二种元素组成的物质中,沸点最高的是,原因是,该物质的分子构型为,中心原子的杂化轨道类型为。
(4)图A中的双原子分子中,极性最大的分子是。
(5)k的分子式为,中心原子的杂化轨道类型为,属于分子(填“极性”或“非极性”)。