短周期元素Q、W、X、Y、Z的原子序数依次增大,X元素的颜色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍,W、Z原子的最外层电子数相同,Z元素的核电荷数是W的2倍,Y是地壳中含量最多的金属元素。下列说法不正确的是 ( )
| A.工业上常用电解的方法制备X、Y的单质 |
| B.元素Q和Z能形成QZ2型的共价化合物 |
| C.原子半径的大小顺序:r(X)> r(Y)> r(W)> r(Q) |
| D.元素X、Y的最高价氧化物对应的水化物之间能发生反应 |
某同学进行了如 图所示的实验,由实验现象得到
图所示的实验,由实验现象得到 的结论中正确的是
的结论中正确的是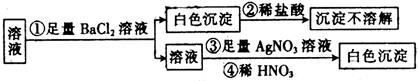
A.原溶液中一定只含有SO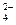 |
B.原溶液中一定含有SO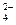 和Cl— 和Cl— |
| C.原溶液中一定只含有Cl— | D.原溶液中可能含有SO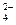 ,也可能含有Cl— ,也可能含有Cl— |
某1.2 mol ·L-1 Fe2 (SO4) 3和2.4 mol·L-1 CuSO4的混合溶液100 mL,最多能溶解铁粉的物质的量为
| A.0.30 mol | B.0.36 mol | C.0.48 mol | D.0.56 mol |
下列实验能达到预期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
将SO2通入溴水,溴水褪色后加热观察能否恢复原色 |
验证SO2漂白的可逆性 |
| B |
将氯水加入淀粉KI溶液中 |
验证C1的非金属性比I强 |
| C |
把铁块和铜块用导线连接插入浓硝酸中 |
组成原电池验证Fe比Cu活泼 |
| D |
加热氯化铵和碘单质的固体混合物 |
分离除去碘单质 |
一定条件下,体积为2L的密闭容器中,1mol A和1mo1 B进行反应:A(g)+3B(g) 2C(g)经2分钟反应达到平衡,此时生成0.2mol C。
2C(g)经2分钟反应达到平衡,此时生成0.2mol C。
下列说法正确的是
A.反应开始至2分钟时,以B浓度变化表示的反应速率为0.05mol/(L.min)
B.反应开始至2分钟时,A的 转化率为5%
转化率为5%
C.若其他条件不变,升高温度,A的体积分数增大,则该反应的△H<0
D.若其他条件不变,增大压强,化学反应速率的变化符合下示意图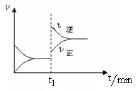
美国罗氏生产的奥司他韦磷酸盐胶囊剂(商品名中国大陆称达菲·港 译特敏福,台湾译为克流感)是市场上唯一的奥司他韦制剂。2009的,由于甲型H1N1在世界范围的扩散,全球掀起一般抢购达菲的风潮。奥司他韦的结构如图;下列说法正确的是
译特敏福,台湾译为克流感)是市场上唯一的奥司他韦制剂。2009的,由于甲型H1N1在世界范围的扩散,全球掀起一般抢购达菲的风潮。奥司他韦的结构如图;下列说法正确的是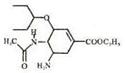
| A.奥司他韦是一种芳香族化合物,分子式为C18H28O4N3 |
| B.1mol该化合物可以和3mol氢气发生加成反应 |
| C.该化合物能发生水解反应,加成反应、氧化反应和消去反应 |
| D.奥司他韦可以和磷酸在一定条件下制取奥司他韦磷酸盐是由于具有碱性基团氨基 |