三氯化铁晶体(FeCl3·6H2O)跟水反应生成的氢氧化铁胶体具有净水作用,三氯化铁被用作净水剂,并且具有实用价值。明矾[KAl(SO4)2·12H2O]也是具有实用价值的净水剂之一,城市自来水厂常用其在常温下对大量的水进行净化。
(1)如果选择适当的分类标准,可以将三氯化铁晶体和明矾这两种不同的物质归为同一类物质,请你来进行划分(只要答出其中两项即可):
①分类标准: ,物质类型名称 。
②分类标准: ,物质类型名称 。
(2)取某浑浊水50 mL盛在烧杯中,再向烧杯中加入适量的明矾粉末并用玻璃棒将水搅拌,发生的现象是
。
(3)食盐水和明矾溶液都是无色、澄清、透明的液体。对这两种液体进行鉴别方法很多,如果不用任何试剂进行鉴别,有关的方法、现象和结论是
。
海水是人类资源的宝库, “海水晒盐”是获取食盐的重要来源。食盐既是一种生活必需品,也是一种重要的工业原料。以食盐为原料可以得到多种产品。
⑴工业上用NaCl制备金属钠的化学方程式是。
⑵工业上主要通过电解饱和氯化钠溶液的方法获得氢氧化钠。
①该过程中阴极的产物是 ;阴极反应为:
;阴极反应为:
②阳极反应式为,检验该电极反应产物的方法是:
。
③当阴极上收集到标准状况下气体22.4L时(假设产生的气体完全被收集),则电路中通过电子的数目为NA。
⑶电解氯化钠稀溶液可以制备“84”消毒液,若通电时产生的氯气被溶液完全吸收,且最终所得消毒液仅含一种溶质,请写出相应的化学方程式:
(用一个方程 式表示)。
式表示)。
⑷海水电解制得的氢气用于合成氨,某合成氨厂生产流程如下: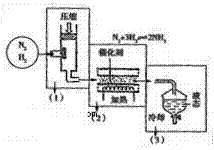
①在第(1)个设备中先把N2 、H2压缩的目的是 :
: 。
。
②在第(3)个设备中用冷却的方法分离出其目的是:
。
Ⅰ、北京时间11月1日清晨5时58分07秒,中国“ 长征二号F”遥八运载火箭在酒泉卫星发射中心载人航天发射场点火发射,火箭的第三级使用的推进剂是液氢和液氧。
长征二号F”遥八运载火箭在酒泉卫星发射中心载人航天发射场点火发射,火箭的第三级使用的推进剂是液氢和液氧。
已知下面在298K时的热化学方程式:
2H2(g)+O2(g)=2H2O(l);ΔH=–571.6kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH=–890.3kJ·mol-1
C(S)+O2(g)=CO2(g);ΔH=–393.5kJ·mol-1[来
根据上面的热化学方程式完成下列问题:
⑴通过计算说明等质量 的H2、C、CH
的H2、C、CH 4完全燃烧时放出热量最多的是。
4完全燃烧时放出热量最多的是。
⑵根据以上反应,则C(S)+2H2(g)=CH4(g)的焓变ΔH=。
⑶已知H2O(l)=H2O(g);ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气时的热化学方程式:
。
Ⅱ、据统计,发达国家每年由于金属腐蚀造成的直接损失约占全年国民生产总值的2%~4%,远远超出水灾、火灾、风灾、地震等自然灾害造成损失的总和。因此,了解 金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
⑴分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是。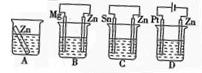
⑵利用下图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于处。若X为锌,开关K置于M处,该电化学防护法称为。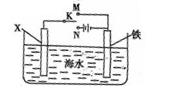
已知A是我们家庭中常见的一种调味剂,其焰色反应呈黄色; E是引起温室效应的主要气体之一;反应①是工业上生产化合物D的反应,反应⑤是实验室鉴定化 合物E的反应。根据下列反应框图填空:
合物E的反应。根据下列反应框图填空: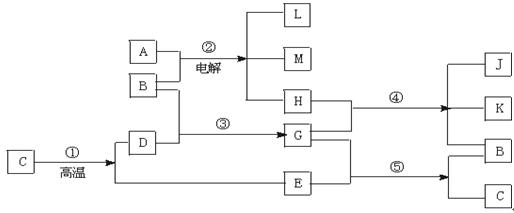
(1)写出有关物质的名称或化学式:
B,C,H。
(2)写出②发生反应的化学反应方程式
。
写出④发生反应的化学方程式,并用双线桥表示出电子转移的方向和数目 。
 现有一包固体可能由下列一种或几种物质组成:CuSO4、NaI、KNO3、NH4Cl、BaCl2、Na2CO3,为了鉴别做以下实验:
现有一包固体可能由下列一种或几种物质组成:CuSO4、NaI、KNO3、NH4Cl、BaCl2、Na2CO3,为了鉴别做以下实验:
(1)将一定量的固体溶于水,得到无色澄清的溶液;
(2)将实验(1)中的溶液分成三份:在第一份溶液中加入足量的氢氧化钠溶液并加热,生成一种能使湿润红色石蕊试纸变蓝色的气体;在第二份溶液中滴入足量的稀盐酸,生成一种能使澄清石灰水变浑浊的气体;在第三份溶液中加入新制的氯水后,溶液变成深黄色,加入四氯化碳后振荡、静置,下层液体呈紫 红色。试
红色。试 回答下列问题:
回答下列问题:
(1)原固体混合物中一定存在的物质是,一定不存在的物质是 。
(2)实验(2)中第一份溶液与氢氧化钠溶液共热时发生的反应方程式
。
(1)根据下列几种粒子的结构示意图,回答问题: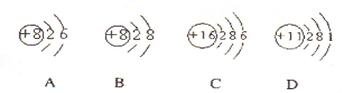
①其中属于阴离子的是 ,属于金属元素的是 。(填编号)
②试写出A、C、D三种元素形成的一种化合物在水溶液中的电离方程式:。
(2)已知氢元素有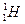 、
、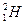 、
、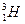 三种核素,氧
三种核素,氧 元素也有
元素也有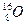 、
、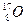 、
、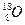 三种核素,则它们所形成的水分子共有种。
三种核素,则它们所形成的水分子共有种。
(3)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下: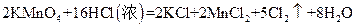
①在该反应中,氧化剂是,还原剂是 。
②当有0.20 mol电子发生转移时,生成氯气的体积为L(标准状况)