已知HNO3(浓)和S加热生成NO2,该反应的含硫产物肯定不是 ( )
| A.H2S | B.SO2 | C.SO3 | D.H2SO4 |
下列化学用语所表示的粒子中,氧化性最强的是()
A.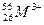 |
B.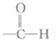 |
C.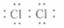 |
D.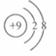 |
下列物质中有毒且有色的气体是()
| A.CO | B.NO | C.白磷 | D.Cl2 |
现有Cu和Cu2O的混合物,将其分成两等份。一份用足量氢气还原,测得反应后固体质量减少8.0g;另一份加入500 mL稀硝酸,固体恰好完全溶解,且收集到标准 状况下8.96LNO(假定无其它气体生成)。则所用硝酸的物质的量浓度为()
状况下8.96LNO(假定无其它气体生成)。则所用硝酸的物质的量浓度为()
| A.3.2 mol/L | B.4.4mol/L | C.5.2mol/L | D.6.0mol/L |
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,pH值随溶液体积变化的曲线如右图所示。下列判断不正确的是()
| A.曲线Ⅰ代表盐酸,曲线Ⅱ代表醋酸 |
| B.溶液中水的电离程度由大到小的顺序:a>b>c |
| C.溶液的导电性由强到弱的顺序:a>b>c |
| D.a点溶液中加入少量醋酸钠固体,溶液酸性降低 |
下列有关图像的分析正确的是()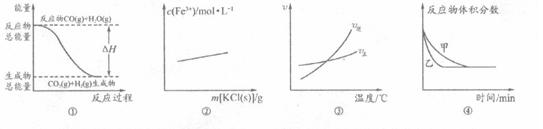
A.图①表示反应“CO(g)+H2O(g) CO2(g)+H2(g)”中的△H大于0 CO2(g)+H2(g)”中的△H大于0 |
B.图②可表示反应“3KSCN+FeCl3 Fe(SCN)3+3KCl”向正反应方向移动 Fe(SCN)3+3KCl”向正反应方向移动 |
C.图③表示反应“A2(g)+3Br(g) 2AB3(g)”的△H小于0 2AB3(g)”的△H小于0 |
D.图④可表示压强对反应“2A(g)+2B(g) 3C(g)+D(s)”的影响,且乙 3C(g)+D(s)”的影响,且乙 的压强大 的压强大 |