烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含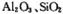 等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫。
等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫。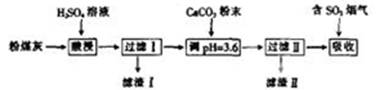
(1) (填“能”或“不能”)用NaOH溶液代替H2SO4溶液。
(2)酸浸时反应的离子方程式为 。
(3)加CaCO3调节溶液的pH至3.6其目的是 。
(4)已知粉煤灰中Al2O3的质量分数为40.8%,制得的碱式硫酸铝[Al2(SO4)x(OH)6-2x]中x=1.5。某实验小组取80.0g粉煤灰进行上述实验,假设在整个过程中铝的损耗率为10%,则可制得碱式硫酸铝的质量为 。
Ⅰ.下面是s能级p能级的原子轨道图,试回答问题: s电子的原子轨道呈形,每个s能级有个原子轨道;p电子的原子轨道呈形,每个p能级有个原子轨道。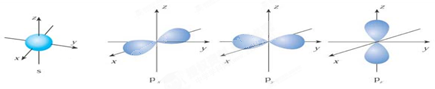
Ⅱ.写出下列元素基态原子的电子排布式:
(1)Ca。
(2)Kr。
(3)Co。
(4)Ge。
已知A、E、I、L是常见的非金属单质,其中A为淡黄色固体;Z是常见的金属单质,B的相对分子质量比A大32,C的相对分子质量比B大16,Y是一种常见的液体,J是磁性氧化铁,D、H、K均是重要的化工产品;X是结构有待探究的一种新型分子,其组成元素的相对原子质量相差18,下列框图中部分反应条件已略去。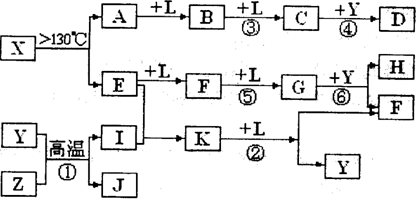
试回答下列问题:
(1)E的结构式为___________,在反应①、②、③、④、⑤、⑥中属于非氧化还原反应的是___________。(填序号)
(2)写出反应②的化学方程式:_________________________________________
(3)若有G、F的混合气体通入足量烧碱溶液,气体全部被吸收,则气体G、F的物质的量之比应满足n(G)︰n(F)____________________
(4)J与过量H的稀溶液反应的离子方程式为___________________________________。
(5)t℃时,将2mol E和1mol I通入体积为2L的恒温密闭容器中发生反应,2min后达到平衡n(K)=0.2mol, 此时保持温度不变,体积减半,则E的体积分数如何变化____________(填“增大”、“不变”、“变小”)
已知2X2(g)+Y2(g) 2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
(1)此反应平衡常数表达式为____________________;若将温度降低到300℃,则反应平衡常数将______________(填增大、减少或不变)。
(2)若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量c kJ,则Z浓度___________Wmol·L-1(填“>”、“<”或“=”),a,b、c之间满足关系___________(用代数式表示)。
(3)能说明反应已达平衡状态的是_____________________(从下列选项中选择)。
a.浓度c(Z)=2c(Y2) b.容器内压强保持不变
c.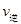 (X2)=2
(X2)=2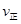 (Y2) d.容器内的密度保持不变
(Y2) d.容器内的密度保持不变
(4)若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2mol X2和lmol Y2达到平衡后,Y2的转化率将___________(填“变大”、“变小”或“不变”)。
几种短周期元素的原子半径及主要化合价见下表:
分析上表的有关数据,并结合已学过知识,请用化学用语到答下列问题。
(1)写出D元素在周期表中的位置___________________。
(2)含20克F的最高价氧化物的水化物的稀溶液与足量B的氢化物的稀溶液反应放出热量a kJ,请写出该反应的热化学反应方程式____________________________。
(3)用电子式表示F2C2的形成过程______________________________。
(4)BA2能与盐酸反应得到黄绿色气体,试写出化学反应方程式:__________________,
B、C、F的最高价氧化物对应的水化物形成溶液,浓度均为0.1mol/L时,pH由大到小的顺序为___________________。
(5)lmol F2A2与水反应生成的溶液与lL 0.5mol/LEB3溶液反应的离子方程式为
______________________________。
某无色溶液中含有K+、Cl-、OH-、 、
、 ,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
请你根据实验操作及现象分析完成下列各题:
(1)图中现象a、b、c表明检验出的阴离子分别是:
a_________________, b___________________,c_____________________。
(2)白色沉淀A加过量试剂②发生反应的离子方程式是:___________________。
(3)无色溶液A加试剂③的主要目的是:_____________________________________。
(4)白色沉淀A若加试剂③而不加试剂②对实验结果有无影响(选填“有影响”、“无影响"或“无法确定”)____________________________。
(5)气体B通入试剂④中发生反应的离子方程式是:____________________________。