(10分)聚合硫酸铁(SPFS)是一种新型的饮用水处理剂和城市污水净化剂,其化学组成可表示为[Fe2(OH)n(SO4)3 - 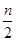 ]m 。某研究小组将聚合硫酸铁在一定条件下加热完全分解,对所得气体产物和固体产物进行实验探究。请利用实验室常用仪器、用品和以下试剂完成验证和探究过程(已知SO3的熔点为16.8 ℃)。
]m 。某研究小组将聚合硫酸铁在一定条件下加热完全分解,对所得气体产物和固体产物进行实验探究。请利用实验室常用仪器、用品和以下试剂完成验证和探究过程(已知SO3的熔点为16.8 ℃)。
试剂:1.0 mol·L-1的盐酸、1.0 mol·L-1的KMnO4溶液、 0.1 mol·L-1的BaCl2溶液、20%的KSCN溶液、品红溶液、蒸馏水、冰水。
(1)聚合硫酸铁中铁元素的化合价是________
(2)固体产物成分的探究
【实验设计】
| 实验步骤 |
现象 |
| 步骤1:取适量的固体产物于试管中,加入足量1.0 mol·L-1的盐酸,充分振荡使固体完全溶解。 |
固体溶解,没有观察 到气泡,溶液呈黄色 |
| 步骤2:取少量步骤1所得溶液于试管中,加入适量20%的KSCN溶液振荡 |
溶液呈血红色 |
| 步骤3:另取少量步骤1所得溶液于试管中,滴入少量1.0 mol·L-1的KMnO4溶液,振荡。 |
KMnO4的紫红色不褪去 |
【思考与判断】 根据上面的信息,可以确定固体产物的成分是________;
步骤1中发生反应的离子方程式为
(3)气体产物成分的探究(不考虑水蒸气)
【提出假设】 假设1:所得气体的成分是SO3 假设2:所得气体的成分是SO2、O2
假设3:所得气体的成分是
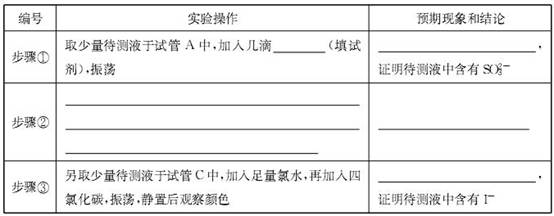
【设计实验方案,验证假设】按下表的实验步骤写出预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1:将少量气体产物通入盛有适量品红溶液的试管中,观察溶液的颜色变化,然后加热再观察溶液的颜色变化 |
① ② |
| 步骤2:将气体产物缓缓通过浸在冰水中的U形管(如图),然后在U形管中加入适量0.1 mol·L-1的BaCl2溶液,充分振荡 |
结合步骤1中的② |
某课外活动小组拟用下列实验装置探究氯气与氨气之间的反应。其中A、B分别为氨气和氯气的发生装置;C为纯净、干燥的氯气与氨气反应的装置。表中的三个备选装置则是为完成实验必须的设备。各装置之间用橡胶管连接。请回答下列问题:



(1).若NH3从左向右流动,Cl2从右向左流动,则装置的正确连接顺序为:A、_____、_____、_____、_____、B(请将C、D、E、F填在相应的横线上)
(2)正确连接装置后,如何检验A装置的气密性____________________________________。
(3)装置A中的烧瓶内试剂可选用________(选填以下选项的代号)。
A.烧碱 B.浓硫酸 C.生石灰 D.五氧化二磷
(4)装置B中发生反应的离子方程式是______________________________________。
(5)反应开始后,C装置内产生白烟,试写出C内的化学反应方程式___________________。
(6)为使NH3与Cl2的混合更充分,Cl2应从C装置的______口进入(填“a”、“b”、“c”)
(7)该装置是否还存在着缺陷______(填“是”、“否”),如果有,其相应的改进措施是________________________________(如果没有,则不填该空)。
过碳酸钠(2Na2CO4·3H2O)是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下:
试回答下列问题:
(1)过碳酸钠溶于水后所得溶液显(填“酸性”、“碱性”或“中性”)。请用离子方程式表示:______________________。
(2)操作①需要的玻璃仪器有(填写仪器名称)。
(3)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
①要检验工业纯碱中杂质的存在,最好选用下列试剂中的__________(选填序号)。
a. 氢氧化钡溶液b. 稀硝酸 c. 硫氰化钾溶液d. 硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若观察到说明装置不漏气。
③装置A的作用是,装置C中的试剂为。
④某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要?(选填“必要”或“不必要”),判断的理由是。
某化学小组设计如图实验装置(夹持装置略去)制备Cl2并探究氯气的相关性质:
(1)若装置A中的固体药品为KClO3,则反应中每生成3mol Cl2 时转移电子的物质的量
为。
(2)装置B既能除去氯气中的氯化氢,还能检测实验过程中装置C是否发生堵塞。若C中发生堵塞,B中将观察到的现象是。
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是,。
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。请简述能说明氯、溴、碘非金属性强弱的实验操作及现象。
(5)用化学方程式说明装置F的作用。
(6)甲同学提出,装置F中的试剂可改用足量的Na2SO3溶液,乙同学认真思考后认为此法不可行。请用离子方程式解释乙认为不可行的原因:。
PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
| 熔点/℃ |
沸点/℃ |
密度/g·mL-1 |
其他 |
|
| 黄磷 |
44.1 |
280.5 |
1.82 |
2P(过量)+3Cl2 2PCl3;2P+5Cl2 2PCl3;2P+5Cl2 2PCl5 2PCl5 |
| PCl3 |
—112 |
75.5 |
1.574 |
遇水生成H3PO3和HCl,遇O2生成POCl3 |
| POCl3 |
2 |
105.3 |
1.675 |
遇水生成H3PO4和HCl,能溶于PCl3 |
(一)制备:RU 图是实验室制备PCl3的装置(部分仪器已省略)
(1)仪器乙的名称____________。
(2)实验室用漂白粉加浓盐酸制备Cl2的化学方程式:_______________________ 。
(3)碱石灰的作用是____________________。
(4)向仪器甲中通入干燥Cl2之前,应先通入一 段时间的CO2,其目的是____________________。
(二)提纯:
(5)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过_________________(填实验操作名称),即可得到PCl3的纯品。
(三)分析:
测定产品中PCl3纯度的方法如下:迅速称取4.200 g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的0.1000 mol/L 20.00 mL 碘溶液,充分反应后再用0.1000 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗10.00 mL Na2S2O3溶液。
已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应。
(6)根据上述数据,该产品中PCl3的质量分数为____________________ 。若滴定终点时俯视读数,则PCl3的质量分数_______(偏大、偏小、或无影响)
某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验,请回答下列问题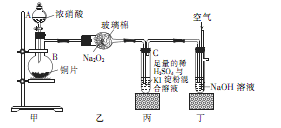
(1)装置甲中盛放浓硝酸的仪器A的名称是,仪器B中发生反应的化学方程式为
(2)完成下面表格中的空白
(3)取下装置丙中的试管C,向其中滴加足量的Na2SO3溶液,溶液颜色褪去,该过程中发生反应的离子方程式为。反应后的溶液中主要含有SO32—、SO42—、I—等阴离子,请填写鉴定SO32—、SO42—和I—的实验报告。
限选试剂:2mol·L—1HCl、1mol·L—1H2SO4、1mol·L—1BaCl2、1mol·L—1Ba(NO3)2、CCl4、新制饱和溴水、新制饱和氯水。