下列十二种物质中:Fe、 CaO、SO3、盐酸、硫酸、KOH溶液、NH4HCO3、CCl4、NH3·H2O 、HF、BaSO4、熔融的KCl. 其中属于强电解质、弱电解质、非电解质的物质种类依次为:
| A.5、2、2 | B.7、3、2 | C.6、2、4 | D.5、3、4 |
某温度下,CO2饱和溶液的浓度是0.03mol/L,其中1/3的CO2转变为H2CO3,而H2CO3仅有0.1%发生如下电离:H2CO3 H++HCO3—,则溶液的pH约为( )
H++HCO3—,则溶液的pH约为( )
| A.3 | B.4 | C.5 | D.6 |
已知相同条件下,HClO的电离常数小于H2CO3的一级电离常数(Ka)。为了提高氯水中HClO的浓度,可加入( )
| A.NaCl(s) | B.CaCO3(s) | C.H2O | D.NaOH(s) |
25℃时,水中存在电离平衡:H2O H++OH-。下列关于水的说法,不正确的是( )
H++OH-。下列关于水的说法,不正确的是( )
| A.水的电离是吸热过程 |
| B.向水中加入少量稀硫酸,c(H+)增大,KW不变 |
| C.含H+的溶液显酸性,含OH-的溶液显碱性 |
| D.水是极弱的电解质,在50℃时水的pH小于7 |
水的电离平衡曲线如下图所示。下列说法正确的是 ( )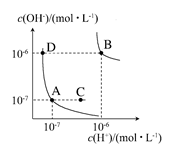
| A.图中对应点的温度关系为A>B |
| B.水的电离常数KW数值大小关系为B>D |
| C.温度不变,加入少量NaOH可使溶液从C点变到A点 |
| D.在B点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显酸性 |
有关水的电离平衡的说法正确的是( )
| A.水的离子积通常用KW来表示,随温度变化而变化,只适用于纯水,在稀盐酸中数值会变大 |
| B.在纯水中加入硫酸会抑制水的电离,加醋酸会促进水的电离 |
| C.盐溶于水对水的电离平衡均没有影响 |
| D.在纯水中加入氢氧化铁固体对水的电离平衡会有微弱的影响 |