亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: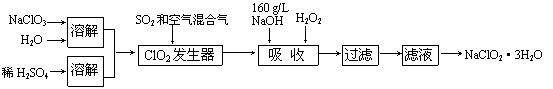
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
请回答下列问题:
(1)发生器中鼓入空气的作用可能是 。
(2)吸收塔内反应的化学方程式为 。
(3)吸收塔的温度不能超过20℃,原因是 。
(4)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(5)从滤液中得到NaClO2•3H2O晶体的实验操作依次是 、 、 过滤、洗涤、干燥。
某兴趣小组依据CO2+2Mg=2MgO+C,推测Mg与SO2在隔绝空气条件下反应后,剩余固体M可能含有MgO、S、MgS、Mg中的一种或几种。为了验证推测,进行以下实验。请回答有关问题。
实验Ⅰ按下图所示进行实验。
(1)实验前需除去镁条表面氧化膜。用简易的物理方法除氧化膜的操作是;
(2)实验室制取二氧化硫的化学方程式为;
(3)上述装置存在不合理之处,请提出1项改进建议;
(4)实验时,先通入SO2直到现象出现后,再点燃酒精灯;此操作目的是。
实验Ⅱ确定固体M的成分。
实验装置如图所示。
将分液漏斗中稀硫酸(足量)
加入到烧瓶中,完全反应后,实验现象如下:
| 装置 |
A |
B |
C |
量气管 |
| 现象 |
有残留 固体 |
产生白色ZnS沉淀 |
溴水 未褪色 |
进入气体 v mL(标况) |
(5)实验时,B装置中反应的化学方程式为;
(6)已知镁的相对原子质量为24,则固体M中金属镁的质量为g;实验前装置内有空气,对金属镁质量的测定结果的影响是(填偏低、偏高、无影响);
(7)依以上实验,可确定固体M的成分有种(填数字)。
某学生探究AgCl、Ag2S沉淀转化的原因。
| 步骤 |
现象 |
| Ⅰ.将NaCl与AgNO3溶液混合 |
产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 |
沉淀变为黑色 |
| Ⅲ.滤出黑色沉淀,加入NaCl溶液 |
较长时间后,沉淀变为乳白色 |
(1)Ⅰ中的白色沉淀是。
(2)Ⅱ中能说明沉淀变黑的的离子方程式是,沉淀转化的主要原因是。
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl。用浓HNO3溶解,产生红棕色气体,部分沉淀未溶解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是。
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀______。
(4)该学生通过如下对照实验确认了步骤Ⅲ中乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化。
| 现 象 |
B:一段时间后,出现乳白色沉淀 |
| C:一段时间后,无明显变化 |

①A中产生的气体是_________。
②C中盛放的物质W是_________。
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S +  +
+ + 2H2O
+ 2H2O  4AgCl +
4AgCl + + 4NaOH
+ 4NaOH
④B中NaCl的作用是_______。
辉铜矿(主要成分为Cu2S)经火法冶炼,可制得Cu和H2SO4,流程如下图所示:
(1)Cu2S中Cu元素的化合价是价。
(2)Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
①粗铜应与直流电源的极(填“正”或“负”)相连。
②铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是。
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经下图所示方法脱除SO2,并制得H2SO4。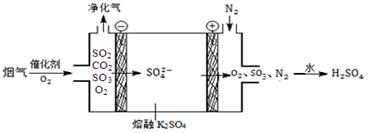
①在阴极放电的物质是。
②在阳极生成SO3的电极反应式是。
(4)检测烟气中SO2脱除率的步骤如下:
i.将一定量的净化气(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
ii.加入浓盐酸,加热溶液至无色无气泡,再加入足量BaCl2溶液。
iii.过滤、洗涤、干燥,称量沉淀质量。
①用离子方程式表示i中溴水的主要作用。
②若沉淀的质量越大,说明SO2的脱除率越(填“高”或“低”)。
某同学分析Zn与稀H2SO4的反应。
(1)该反应的离子方程式是。
(2)制H2时,用稀硫酸而不用浓硫酸,原因是_________。
(3)已知:Zn(s)+1/2O2(g)=ZnO(s) △H=-332kJ/mol
ZnO(s) + H2SO4(aq) = ZnSO4(aq) + H2O(l) △H=-112kJ/mol
H2(g) +1/2 O2(g) = H2O(l) △H=-286kJ/mol
则Zn与稀H2SO4反应生成1mol H2时的反应热△H=kJ/mol。
(4)该同学用如下装置进行实验,分析影响反应速率的因素。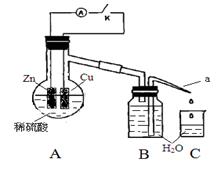
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1 分钟内从a管流出的水滴数,得到的水滴数如下表所示:
| 1分钟水滴数(断开K) |
34 |
59 |
86 |
117 |
… |
102 |
| 1分钟水滴数(闭合K) |
58 |
81 |
112 |
139 |
… |
78 |
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率______(填“快”或“慢”),主要原因是_________。
②由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是_______。
③从能量转换形式不同的角度,分析水滴数86>81、117>112的主要原因是_______。
重晶石(BaSO4)是重要的化工原料,用重晶石制备氢氧化钡晶体[Ba(OH)2·8H2O]的流程如下: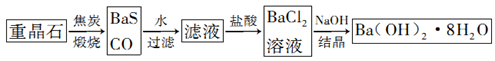
已知:Ba(s)+S(s)+2O2(g) BaSO4(s)ΔH="-1" 473.2 kJ·mol-1
BaSO4(s)ΔH="-1" 473.2 kJ·mol-1
2C(s)+O2(g) 2CO(g) ΔH="-221" kJ·mol-1
2CO(g) ΔH="-221" kJ·mol-1
Ba(s)+S(s) BaS(s) ΔH="-460" kJ·mol-1
BaS(s) ΔH="-460" kJ·mol-1
(1)写出煅烧时发生反应的热化学方程式:。
(2)写出氢氧化钡晶体与氯化铵混合反应的化学方程式:。
(3)为检测煅烧时产生的CO,可将煅烧产生的气体通入PbCl2溶液中,出现黑色沉淀并产生一种无色无味能使澄清石灰水变浑浊的气体,试写出该反应的化学方程式:。
(4)向BaSO4沉淀中加入饱和Na2CO3溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3。发生的反应可表示为BaSO4(s)+ CO32-(aq) BaCO3(s)+ SO42- (aq)。现有0.20 mol BaSO4,加入1.0 L 2.0 mol·L-1饱和Na2CO3溶液处理,假设c(SO42-)起始≈0,平衡时,平衡常数K=4.0×10-2,求反应达到平衡时发生转化的BaSO4的物质的量。(不考虑溶液体积变化与离子水解,写出计算过程,结果保留2位有效数字)
BaCO3(s)+ SO42- (aq)。现有0.20 mol BaSO4,加入1.0 L 2.0 mol·L-1饱和Na2CO3溶液处理,假设c(SO42-)起始≈0,平衡时,平衡常数K=4.0×10-2,求反应达到平衡时发生转化的BaSO4的物质的量。(不考虑溶液体积变化与离子水解,写出计算过程,结果保留2位有效数字)
(5)试从平衡的角度解释BaSO4可转化为BaCO3的原因:。