(1)将反应2H2(g)+O2(g)=2H2O(1) △H<0,以KOH溶液为电解质溶液,设计一个原电池,其负极反应为: 。
(2)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则: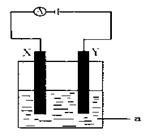
①若X和Y均为惰性电极,a为CuSO4溶液,则电解时的化学反应方程式为: 。
通过一段时间后,向所得溶液中加入0.2molCuO粉末,恰好恢复电解前的浓度和pH,则电解过程中转移的电子的物质的量为 。
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为 。
四种常见的短周期非金属元素在周期表中的相对位置如下所示,其中乙元素原子核外最外层电子数是其电子层数的3倍。
| 甲 |
乙 |
|
| 丙 |
丁 |
请用化学用语回答:
(1)丙在元素周期表中的位置是。
(2)丁单质的电子式是。
(3)乙的两种常见单质分别是、。
(4)甲、乙、丙、丁的气态氢化物水溶液显酸性的是、___________。
(5)氢元素和乙组成的化合物中,既含有极性共价键又含有非极性共价键的是____________ (填化学式)。此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为。
(6)电解丙的饱和钠盐溶液的离子方程式为。
(7)若甲的元素符号为X。已知:①X2(g)+2O2(g)===X2O4(l) ΔH=-19.5 kJ·mol-1;
②X2H4(l)+O2(g)===X2(g)+2H2O(g)ΔH=-534.2 kJ·mol-1。
则液态X2H4和液态X2O4反应生成气态X2和气态H2O的热化学方程式为。
硼元素、钙元索、铜元素在化学中有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用。
(1)已知CaC2与水反应生成乙炔.请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl榕液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为。其在酸性溶液中不跪定,可发生歧化反应生成Cu2十和Cu,但CuO在高温下会分解成Cu2O,
试从结构角度解释高温下CuO为何会生成Cu2O:。
②CaC2中C22-与O22+互为等电子体.1molO22+中含有的π键数目为。
③乙炔与氢氰酸反应可得丙烯睛(H2C=CH一C≡N)。丙烯腈分子中碳原子轨道杂化类型是,构成丙烯腈元素中第一电离能最大的是(填元素符号)。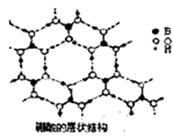
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢健相连(如上图〕.则1 mo1H3BO3的晶体中有mol氢键。硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少[B(OH)4]一和H+,则[B(OH)4]一含有的化学键类型为
(3)Cu3N的晶胞结构如图,N3-的配位数为。Cu+半径为a cm,N3-半径为bcm,Cu3N的密度为___g/cm3,(阿伏加德罗常数用NA表示)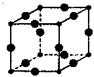
【化学——物质结构与性质】太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。其材料除单晶硅,还有铜铟镓硒等化合物。
(1)镓的基态原子的电子排布式是。
(2)硒为第4周期元素,相邻的元素有砷和溴,则3种元素的第一电离能从大到小顺序为(用元素符号表示)。
(3)气态SeO3分子的立体构型为________。
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___________。
(5)与镓元素处于同一主族的硼元素具有缺电子性,其化合物往往具有加合性,因而硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,则[B(OH)4]-中B的原子杂化类型为;
(6)金属Cu单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,反应的离子方程式为;
(7)一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为_____________,若该晶胞的边长为a pm,则合金的密度为_________ g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
短周期元素形成的常见非金属固体单质 A 与常见金属单质 B,在加热条件下反应生成化合物 C,C 与水反应生成白色沉淀 D 和气体 E,D 既能溶于强酸,又能溶于强碱。E 在足量空气中燃烧产生刺激性气味的气体 G,G 在大气中能导致酸雨的形成。E 被足量氢氧化钠溶液吸收得到无色溶液 F。溶液 F 在空气中长期放置发生反应,生成物之一为 H。H 与过氧化钠的结构和化学性质相似,其溶液显黄色。请回答下列问题:
(1)组成单质 A 的元素在周期表中的位置。
(2)B 与氢氧化钠溶液反应的化学方程式为:_____________________。
(3)G 与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为__________,当生成 2mol 二氧化氯时,转移电子___________mol。
(4)溶液 F 在空气中长期放置生成 H 的化学方程式为:________________________。
(5)H 的溶液与稀硫酸反应产生的现象为_______________________。
恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)="13" mol,n (NH3)="6" mol, a="________" 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。n(NH3) __________。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)= _____。
(4)原混合气体中,a:b=。
(5)将1molN2和3molH2合成NH3反应时,下列叙述能说明该反应已达到化学平衡状态的是(填标号)_________ ;
| A.容器内的总压强不随时间而变化 |
| B.反应后混合气体的密度不再发生变化 |
| C.三种气体的浓度相等且保持不变 |
| D.NH3的分解速率与生成速率相等 |
E、混合气体的平均相对分子质量不再发生变化