(10分)ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与纯净的氯气反应 2NaClO2+Cl2═2ClO2+2NaCl
如图是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有CCl4液体。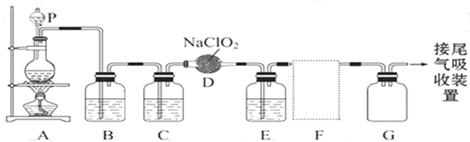
(1)仪器P的名称是_______
(2)写出装置A中烧瓶内发生反应的化学方程式:____________________________
(3)E装置中所盛试剂的作用是_____________________________
(4)F处应选用的收集装置是_______(填序号),其中与E装置导管相连的导管口是______________(填接口字母)。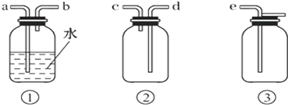
(5)以下是尾气吸收装置,能用于吸收多余ClO2气体,并能防止倒吸的装置的是_________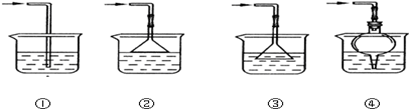
A.①② B.②③ C.③④ D.②④
(6)若用100mL 2mol•L-1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量 是_______(填序号)。
A.>0.1mol B.0.1mol C.<0.1mol D.无法判断.
(7) ClO2也可由KClO3在H2SO4溶液存在下与Na2SO3反应制得。请写出反应的离子方程式:___________________________________________________________________________。
学生为探究苯与溴发生反应的原理,用如图所示装置进行了实验。根据相关知识回答下列问题: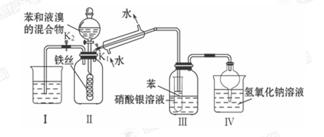
(1)实验开始时,关闭K2,开启K1和分液漏斗活塞,滴加苯和液溴的混合液,反应开始。过一会儿,在装置Ⅲ中可能观察到的现象除小试管中有气泡、液体变棕黄外还可能观察到的现象是_____ 。
(2)整套实验装置中能防止倒吸的装置有__________(填装置序号)。
(3)你认为通过该实验,有关苯跟溴反应的原理方面能得出的结论是__________ 。
(4)本实验能不能用溴水代替液溴? ______________ 。
(5)采用冷凝装置,其作用是_________________ 。
(6)Ⅲ装置中小试管内苯的作用是_____________ 。
(7)若实验时,无液溴,但实验室有溴水,该实验_____ (填“能”或“不能”)做成功
(5分)草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,做了如下实验:
①称取W g纯草酸晶体,将其配制成100.0 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为a mol•L-1的KMnO4标准溶液进行滴定,滴定时发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=====K2SO4+2MnSO4+l0CO2 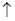 +8H2O
+8H2O
请回答:
(1)滴定时,将KMnO4标准液装在滴定管中,操作时用手拿锥形瓶。
(2)若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会(填“偏大”“偏小”或“不变’’)。
(3)假设滴定终点时,用去V mL KMnO4溶液,则待测草酸溶液的物质的量浓度为mol•L-1。
某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,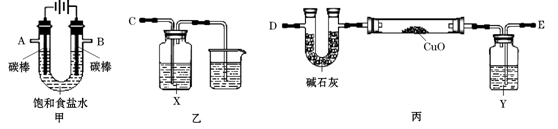
并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时验证氯气的氧化性。
(1)写出甲中反应的离子方程式。
(2)为完成上述实验,正确的连接顺序为A连,B连(填接口字母)。
(3)乙装置中X试剂可以是,丙装置中Y试剂的作用是。
(4)测定Cu的相对原子质量。将w g CuO置于硬质玻璃管中,足量的H2与之充分反应后,按以下两个方案测得的数据计算Cu的相对原子质量。
| 方案 质量 |
方案一 |
方案二 |
| U型管+固体 |
硬质玻璃管+固体 |
|
| 反应前质量/g |
a |
c |
| 完全反应后质量/g |
b |
d |
你认为方案较佳,另一个方案得到的Cu的相对原子质量会(填“偏低”、“偏高”)。按较佳方案计算,得到Cu的相对原子质量是。
下图是两个实验装置(铁架台等辅助仪器略去未画)②原混合物中碳酸钠的质量分数。
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液450 mL.根据这两种溶液的配制情况回答下列问题:
(1)如图 所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是,
所示的仪器中配制溶液肯定不需要的是 (填序号),仪器C的名称是,
本实验所需玻璃仪器E规格为 mL。
(2)下列操作中,容量瓶所不具备的功能有 (填序号)。
A.配制一定体积准确浓度 的标准溶液 的标准溶液 |
B.长期贮存溶液 |
| C.用来加热溶解固体溶质 | D.量取一定体积的液体 |
(3)在配制NaOH溶液实验中其他操作均正确。若定容时仰视刻度线,则所配溶液浓度0.1 mol/L(填“大于”“等于”或“小于”,下同)。若NaOH溶液未冷却即转移至容量瓶定容则所配溶液浓度
0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为mL(计算结果保 留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。
留一位小数)。如果实验室有10 mL、25mL、50 mL量筒,应选用 mL规格的量筒最好。