FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
1.实验需要90mL 0.1mol/L FeBr2溶液
(1)配制FeBr2溶液除烧杯、量筒、胶头滴管外还需的玻璃仪器是 、
(2)下列有关配制过程中说法错误的是 (填序号)。
A用电子天平称量质量为1.944g的FeBr2.
B将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
C洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
D.容量瓶贴签存放配好的FeBr2溶液
E.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II. 探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中; 假设2:Fe2+被Cl2氧化成Fe3+。
(1)请你完成下表,验证假设:
| 实验步骤、预期现象 |
结论 |
| ①溶液中加入适量四氯化碳, |
假设1正确 |
| ②向溶液中加入 |
假设2正确 |
若假设1正确,从实验①中分离出Br2的实验操作名称是 ____________ ;
(2)实验证明:还原性Fe2+> Br-,请用一个离子方程式来证明: _________________ ;
(3)若在50mL上述FeBr2溶液中通入5×10-3molCl2,反应的离子方程式为 。
比较甲烷与氯气、乙烯与溴的反应,以及甲烷、乙烯在空气中燃烧的现象,按要求填写下列表格
| 反应物 |
反应类型 |
反应条件 |
生成物(写结构简式) |
现象 |
| 甲烷、氯气 |
① |
④ |
||
| 乙烯、溴 |
② |
⑤ |
||
| 甲烷、氧气 |
③ |
|||
| 乙烯、氧气 |
⑥ |
1)2)
3)4)
5)6)
下表是元素周期表的一部分
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
O |
| 1 |
||||||||
| 2 |
D |
|||||||
| 3 |
B |
C |
E |
|||||
| 4 |
A |
(1)写出元素符号: B.C、D 、E;
、E;
(2)D-离子结构示意图,B+离子结构示意图,
人类的生活和生产活动,都离不开能源。在石油、电能、风能、煤碳、天然气、秸杆、水力、水煤气这些能源中,属于“二级能源”的(两种)是_____属于“不再生能源”的(三种)是____。
在 H,
H, H,
H,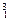 H,
H,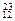 Mg,
Mg,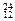 Mg,
Mg,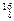 O,
O,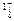 O,
O, O中
O中
(1)共有______种元素,______种原子,中子数最多的是。
D218O的相对分子质量是______。
(2)和互为同位素
和的质量数相等,但不能互称同位素
和的中子数相等,但质子数不等,所以不是同一种元素
在含有Cl-.Br-.I- 的溶液中,已知其浓度均为0.1 mol/L,而AgCl.AgBr.AgI的浓度积(mol2/L2)分别为:1.6×10-10.4.1×10-15.1.5×10-16。若向混合溶液中逐滴加入AgNO3溶液并充分搅拌时,首先析出的沉淀是_______________,最后析出的沉淀是_________;当AgBr沉淀开始析出时,溶液
的溶液中,已知其浓度均为0.1 mol/L,而AgCl.AgBr.AgI的浓度积(mol2/L2)分别为:1.6×10-10.4.1×10-15.1.5×10-16。若向混合溶液中逐滴加入AgNO3溶液并充分搅拌时,首先析出的沉淀是_______________,最后析出的沉淀是_________;当AgBr沉淀开始析出时,溶液 中Ag+的浓度是___________________
中Ag+的浓度是___________________