用9mol/L的浓硫酸稀释成 0.9mol/L的稀硫酸 100mL ,回答下列问题:
(1)配制操作可分解成如下几步,以下正确的操作顺序是_____________________
A向容量瓶中注入少量蒸馏水,检查是否漏水
B用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D.根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线1~2 cm
(2)如果实验室用98%的浓硫酸(密度为1.8g·cm-3 ) 配制3.6 mol·L-1的稀硫酸250mL。计算用量简量取所需浓硫酸的体积为_____________mL。
(3)由于错误操作, 使得到的浓度数据比正确的偏大的是___________(填写序号)。
A.使用容量瓶配制溶液时, 俯视液面定容后所得溶液的浓度
B.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
C.容量瓶用蒸馏水洗净,没有烘干
D.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
E.把配好的溶液倒入用蒸馏水洗净而未干的试剂瓶中备用
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为_____________________________________________________;
(2)实验过程中,装置B、C中发生的现象分别是__________________、____________________,这些现象分别说明SO2具有的性质是________和________;装置B中发生反应的离子方程式为_______________________;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象__________________________________________________________;
(4)尾气可采用________溶液吸收。
(Ⅰ)某无色溶液中可能含有Na+、SO42— 、MnO4—、 、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
、Cl— 、Br—、中的若干种,依次进行下列实验。观察到现象如下:
①用pH试纸检验,溶液pH>7;
②向溶液中滴加氯水,无气体产生,再加入CCl4振荡、静置,CCl4层呈橙红色,用分液漏斗分液;
③向分液后的水溶液中加入AgNO3和HNO3混合液,有白色沉淀产生。
④另取原溶液少量加入Ba(NO3)2和盐酸的混合液,产生白色沉淀。
回答下列问题:
(1)溶液中肯定含有的离子是;肯定没有的离子是。
⑵写出步骤②中的离子方程式。
(Ⅱ)SO2气体通入滴有酚酞的NaOH溶液,红色逐渐褪去,可能的原因:
①②。
简述设计实验证明:。
孔雀石的主要成分为Cu2(OH)2CO3还含少量二价铁和三价铁的氧化物及硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图: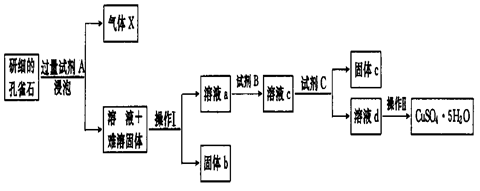
(1)试剂A的化学式是__________;操作I的名称是_________;操作Ⅱ用到的仪器有
酒精灯、玻璃棒、_________、坩埚钳和三角架。
(2)生成气体X的化学方程式为 。
(3)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B最好选用_______(填选项序号)。
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
写出相应反应的离子方程式:。
(4)已知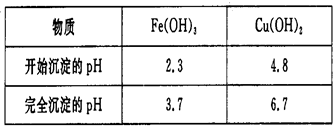
试剂C的使用是为了调节溶液的pH,使Fe3+转化为沉淀予以分离。试剂C宜选用 ___________(填选项序号);
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
为完全除去溶液c中的Fe3+而又不使Cu2+沉淀,则应调节溶液pH的范围为_________。
(5)请设计一种实验方案检验溶液中Fe3+是否完全除去(写出操作步骤、现象和结论)______。
无水CuSO4在一定条件下发生如下反应:
有人设计通过实验测定反应生成的SO3、SO2和O2,并经过计算确定该条件下分解反应方程式各物质的化学计量数,实验所需仪器装置如图所示。
实验测得数据及有关结果如下:
①准确称量无水CuSO46.0g。
②测出量筒中水的体积后,折算成排水的气体在标准状况下的体积为280ml。
③干燥管中的质量在实验结束时增加了3.2g。
④实验结束时,装置F中的溶液变成Na2SO4溶液(不含其他杂质)。
请回答如下问题:
已知气体从左向右的流向,上述仪器装置接口的连接顺序是a →ji→f e →c d →h g→ b
(1)装置F的作用是_____________,装置D的作用是_______________。
(2)首先应计算的物质是______________。
通过计算推断,该条件下反应的化学方程式是_____________________。
(3);(填序号)____________。
“化学多米诺实验”是利用化学反应中气体产生的压力,使多个化学反应依次发生。下图所示就是一个“化学多米诺实验”,其中A~F装置中分别盛放的物质为:
| A.稀硫酸; | B.锌粒; | C.某溶液; | D.CaCO3固体;E、滴有紫色石蕊试液的蒸馏水;F、足量的澄清石灰水 |

请回答下列问题:
⑴反应开始后,若E中出现红色,F中有白色沉淀生成,则C中的物质可能是(填名称)。
⑵写出下列装置中发生反应的离子方程式: 装置D中:
装置D中: 装置F中:
装置F中:
⑶上图所示的B~F装置中,发生了氧化还原反应的是(填装置编号)。