用2.4mol/L的H2SO4溶液配制100mL浓度为0.2 mol/L的稀H2SO4,回答下列问题:
(1)需要量取2.4 mol/L的H2SO4溶液的体积是 mL。
(2)配制过程有下列几步操作:
A 用量筒量取所需H2SO4溶液的体积,注入盛有适量水的烧杯中,用玻璃棒搅拌,使其混合均匀;
B 将蒸馏水加入容量瓶至液面接近刻度线1cm~2cm处;
C 向烧杯中加入约20mL蒸馏水;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也转移到容量瓶中;
E.用 ① 加水至刻度线;
F.待烧杯中溶液冷却后,沿玻璃棒转移到 ② ;
G.盖好瓶塞,反复颠倒摇匀。
以上各步骤操作的先后顺序是 ③ (填字母)
(3)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48 g。则该溶液浓度
0.2 mol/L(填“大于”“等于”或“小于”)造成此误差的操作可能是
A 定容时俯视容量瓶 B 用量筒取2.4mol/L H2SO4溶液时俯视读数
C 使用容量瓶前未干燥 D.使用的烧杯和玻璃棒未洗涤彻底
E.定容时将蒸馏水洒在容量瓶外面
现有以下5种物质:H2O、SiO2、CaO、Na2O2、Al2O3。
(1)按照不同的分类标准,它们中有一种物质与其它物质有明显的不同,请找出这种物质并写出依据(试写出任意一种合理的分类方法):。
(2)上述物质有些可以两两反应,试写出一个属于氧化还原反应的离子反应方程式____。
(12分)工业制硝酸的主要反应之一是:
(1)若反应起始的物质的量相同,下列关系图错误的是________ (填编号)。
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①反应在第2min到第4min时,O2的平均反应速率为________mol/(L ? min)。
②反应在第2min时改变了条件,改变的条件可能是________ (填编号)。
A 增加O2的浓度 B.升高温度 C.减小压强D.使用催化剂
(3)将一定量铝粉和铁粉的混合物与上述反的稀硝酸充分反应,反应过程中无气体放出(氧化物产生)。在反应结束后的溶液中,滴加5mol/L的NaOH溶液,所加NaOH溶液(mL)与产生的沉淀的物质的量关系如图所示则:
EF段反应的离子方程式是_______________;铝粉与铁粉的物质的量之比是_____________
硝酸溶液中含HNO3的物质的量是__________mol。
(8分)燃煤废气中的氮氧化物 、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等。
(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物。如:
则CH4 ( g)将NO2 (g)还原为N2(g)等的热化学方程式是________________________________
(2)将燃煤废气中的CO2转化为甲醚的化学方程式为:
 。已知在一定压强下,该反应随温度的升高而CO2的转化率降低。则该反应的
。已知在一定压强下,该反应随温度的升高而CO2的转化率降低。则该反应的 ________ 0(填“ >”或“ <”);若用以甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池,则该电池中负极的电极反应式是________________________________,放电过程中溶液的PH________ (填“增大”、“减小”或“不变”)。
________ 0(填“ >”或“ <”);若用以甲醚、空气、氢氧化钾溶液为原料,石墨为电极构成燃料电池,则该电池中负极的电极反应式是________________________________,放电过程中溶液的PH________ (填“增大”、“减小”或“不变”)。
(6分)处理含CN-(其中C为+ 2价)的工业废水常用Cl0_氧化,生成的CNO (其中C为+4价),反应的离子方程式为:
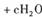 ,上述离子方程式可能的配平系数有多组。请回答:
,上述离子方程式可能的配平系数有多组。请回答:
(1)该离子方程式中e:f的值是________(填选项标号)。
| A.0.5 | B.1 | C.2 | D.不能确定 |
(2)若d="e" =l,则b=________
(3)若反应中转移1.2mol电子,则生成的气体在标况的体积是________。
(12分)A、B、C、D、E五种均为短周期元素,原子序数依次增大。A元素原子最外层电子数是核外电子层数的3倍,A与D同主族,A和D可形成化合物X’X可以使溴水褪色。A元素的单质和C元素的单质化合可生成Y, Y晶体中无分子,也无A、C的离子。A、B元素的单质一定条件下反应生成化合物M,D、B元素的单质反应生成化合物N,化合物M和化合物N的相对分子质量相等,且馅色反应均呈黄色。
请回答下列问题:
(1) 元素C的气态氢化物是________分子(填写“极性”或“非极性”)。
(2) B2D2的电子式是________________
(3) X可以使溴水褪色,该反应的离子方程式是________________________。
(4) 化合物M与化合物N的水溶液反应,若氧化剂与还原剂物质的量之比为1: 1,该反应的离子方程式是________
(5) 右图是BE晶体的一个“晶胞结构”示意图。下列说法正确的是________________。 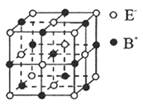
A.与B+距离相等且最近的E_共有6个
B.—个BE晶胞中含有1个B +和1个E_
C.与B+距离相等且最近的B+有8个
D.与B+距离相等且最近的构成的空间结构是正八面体
(6) 将原子序数介于B、C两元素之间的单质、单质B与水反应所得的溶液构成原电池,负极的电极反应式是:O