将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是
| A.c(H+) | B.Ka(HF) |
C. |
D. |
取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是
①金属先熔化
②在空气中燃烧,放出黄色火花
③燃烧后得白色固体
④燃烧时火焰为黄色
⑤燃烧后生成浅黄色固体物质
| A.②⑤ | B.①②③ | C.①④⑤ | D.④⑤ |
著名化学家徐光宪(画面正中),因为在稀土萃取领域取得的卓越成就被誉为“稀土界的袁隆平”;2008年1月9日,胡锦涛主席为其颁发了“国家最高科学技术奖”。稀土元素是指镧系的15种元素,加强钪和钇共17种元素。下列说法正确的是
| A.稀土元素全部是金属元素 |
| B.要萃取出碘酒中的碘可以使用氢氧化钠溶液做萃取剂 |
| C.镧系元素均属于主族元素 |
| D.某些稀土元素在地壳中的含量高于铝 |
向体积为2 L的密闭容器中充入2 mol SO2和1 mol O2,测得起始容器压强为p,一定条件下发生反应:2SO2(g)+O2(g) 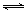 2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入充入2 mol SO3达到新平衡时,容器内的压强为1.4p,则下列说法正确的是
2SO3(g) △H=-196 kJ·mol-1,维持容器温度不变,测得平衡时容器内压强为0.7p,若此时再向容器中充入充入2 mol SO3达到新平衡时,容器内的压强为1.4p,则下列说法正确的是
| A.充入2 mol SO3后,SO2的物质的量增大 |
| B.第一次反应达到平衡时共放出热量176.4 kJ |
| C.充入2 mol SO3达到新平衡时,容器内的压强为1.4p |
| D.降低容器的温度可使新平衡时各物质的体积分数与第一次平衡时相同 |
常温下,向0.1 mol·L-1的CH3COONa溶液中逐滴滴加等浓度的HCl溶液,则下列关系正确的是
| A.c(H+)·c(OH-)=1×10-14 |
| B.c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| C.c(Na+)=c(CH3COOH)+c(CH3COO-) |
| D.c(Na+)=c(Cl-)>c(H+)>c(CH3COO-)>c(OH-) |
下列有关实验操作或实验原理正确的是 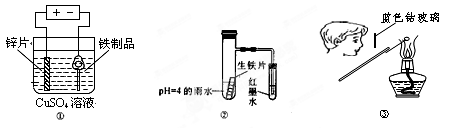
| A.用图①装置在铁制品表面镀锌 |
| B.用蒸发溶剂的方法,将10%的氯化铁溶液变为20%的氯化铁溶液 |
| C.用图②装置验证生铁片在pH=4的雨水中发生析氢还是吸氧腐蚀 |
| D.用图③装置检验K2CO3中的K+ |