(16分)氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。 利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s) Fe3O4(s) + H2(g) △H="a" KJ/mol (Ⅰ)
Fe3O4(s) + H2(g) △H="a" KJ/mol (Ⅰ)
2Fe3O4(s)=6FeO(s) + O2(g) △H="b" KJ/mol (Ⅱ)
下列坐标图分别表示FeO的转化率(图1)和一定温度时,H2生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图2)。
(1)反应:2H2O(g)=2H2(g) + O2(g) ΔH= (用含a、b代数式表示);
(2)在上述循环制氢的过程中FeO的作用是: ;
(3)900°C时,在两个体积均为2L密闭容器中分别投入0.60molFeO和0.20mol H2O(g),甲容器用细颗粒FeO,乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是: ;
②用细颗粒FeO时,H2O (g)的转化率比用粗颗粒FeO时H2O(g)的转化率 (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计算过程)。
(4)在坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注):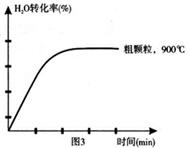
A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。
①元素Y在A、B、C、D、E中所呈现的化合价依次递增,其中只有B为单质;
②常温下将气体D通入水中发生反应,生成E和C;
③工业上可以用A与空气为原料,通过催化氧化法得到C。
请回答以下问题:
(1)B的电子式为,A的结构式为,A分子的空间构型是。
(2)写出②中反应的化学方程式
(3)写出③中反应的化学方程式
将等物质的量的A、B、C、D四种物质混合,发生下列反应:
aA+bB cC(固)+dD。当反应进行一定时间后,测得A减少了n mol,
cC(固)+dD。当反应进行一定时间后,测得A减少了n mol,
B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol,此时达到化学平衡。
(1)该化学方程式中各物质的系数为:a=_____,b=_____,c=_____,d=_____
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的状态为:A_______, B________, C_______
(3)若只升高温度,反应一段时间后测知四种物质的量又相等,则该反应的正反应为________反应(填“放热”或“吸热”)。
实验室制取氯气时,若没有MnO2则用KMnO4代替,据此回答下列问题:
(1)配平该反应
(2)被氧化的HCl与未被氧化的HCl的物质的量之比为
用双线桥法表示出化合价的升降、电子转移数目,指出氧化反应和还原反应及氧化剂和还原剂.
(1)2KClO3 2KCl+3O2↑
2KCl+3O2↑
(2)4P+ O2  2P2O5
2P2O5
某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH- 、NO3-六种离子。甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子、、。 乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量(选填:活性炭或铁粉),可以发生置换反应,离子方程式是,并且能够回收其中的金属 (填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式:,。经过滤后的废水主要含,可用来浇灌农田。