用下图装置(夹持、加热装置已略)进行试验,有②中现象,不能证实①中反应发生的是
| |
①中实验 |
②中现象 |
| A |
铁粉与水蒸气加热 |
肥皂水冒泡 |
| B |
加热NH4Cl和Ca(OH)2的混合物 |
酚酞溶液变红 |
| C |
NaHCO3固体受热分解 |
澄清石灰水变浑浊 |
| D |
石蜡油在碎瓷片上受热分解 |
Br2的CCl4溶液褪色 |
若室温时pH=a的氨水与pH=b的盐酸等体积混和,恰好完全反应,则该氨水中的一水合氨电离的百分比可表示为
| A.10(a+b-12)% | B.10(a+b-14)% | C.10(12-a-b)% | D.10(14-a-b)% |
在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度(mol·L-1) |
0.1 |
0.2 |
0 |
| 平衡浓度(mol·L-1) |
0.05 |
0.05 |
0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z
2Z
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.因该反应的热效应未知,升高温度,平衡常数可能增大,也可能减小
欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO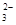 )、c(HCO3-)都减少,其方法是
)、c(HCO3-)都减少,其方法是
| A.通入二氧化碳气体 | B.加入饱和石灰水溶液 |
| C.通入氯化氢气体 | D.加入氢氧化钠固体 |
下列说法或表示方法中正确的是
| A.等质量的硫蒸气和硫磺固体分别完全燃烧,后者放出的热量多 |
| B.氢气的燃烧热为285.8 kJ·mol-1,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l) ΔH=+571.6 kJ·mol-1 |
| C.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l) ΔH<0 |
| D.已知中和热为57.3 kJ·mol-1,若将含0.5 mol H2SO4的溶液与含1 mol NaOH的溶液混合,放出的热量可能大于57.3 kJ |
室温下,若溶液中由水电离产生的c(H+)·c(OH-)=1×10-28mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是
| A.Na+、I-、Cl-、NO3- | B.K+、Ba2+、Cl-、NO3- |
| C.K+、Na+、Br-、F- | D.Fe3+、Na+、NO3-、SCN- |