在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度(mol·L-1) |
0.1 |
0.2 |
0 |
| 平衡浓度(mol·L-1) |
0.05 |
0.05 |
0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z
2Z
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.因该反应的热效应未知,升高温度,平衡常数可能增大,也可能减小
不饱和度(Ω)是衡量有机物分子氢原子饱和程度的尺度,与烷烃及饱和醇相比,分子中每少2个H原子,就有1个Ω,如乙烯、乙醛、苯的不饱和度依次为1、1、4。已知樟脑(C10H16O)的结构如右图,下列4式中与樟脑不属于同分异构体的是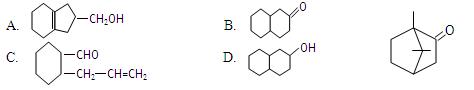
下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是
| A.甲苯反应生成三硝基甲苯 | B.甲苯能使酸性高锰酸钾溶液褪色 |
| C.甲苯燃烧产生带浓烟的火焰 | D.1 mol甲苯与3 molH2发生加成反应 |
据报道:2002年10月26日俄罗斯特种部队在解救人质时使用了一种麻醉作用比吗啡强100倍的氟烷,已知氟烷的化学式为C2HClBrF3,则沸点不同的上述氟烷有
| A.1种 | B.2种 |
C.3种 | D.4种 |
等质量的下列烃完全燃烧,消耗氧气最多的是
| A.CH4 | B.C2H6 | C.C3H6 | D.C6H6 |
下列各组烃的混合物,只要其质量一定,无论它们按什么比例混合,完全燃烧后生成的二氧化碳和水都是恒量的是
| A.C2H2 C2H4 | B.C2H4 C3H8 | C.C3H8 C3H6 | D.C6H6 C2H2 |