NA代表阿伏加德罗常数的值,下列说法正确的是
A.0.1 mol·L-1的Na2SO4溶液中含有Na+和SO 的总物质的量为0.3 mol 的总物质的量为0.3 mol |
| B.常温常压下,22.4LO2所含的原子数小于2NA |
| C.标准状况下,11.2LCH3CH2OH中含有0.5NA个分子 |
| D.1.8g的NH4+ 离子中含有的电子数NA |
X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法正确的是( )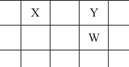
| A.5种元素中,原子半径最大的是W |
| B.Y与Z形成的化合物都可以和盐酸反应 |
| C.Y的简单阴离子比W的简单阴离子还原性强 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
正长石的主要成分为硅酸盐,由前20号元素中的4种组成,化学式为XYZ3W8。其中,只有W显负价。X、Y的最外层电子数之和与Z的最高正价数相等。Y3+与W的阴离子具有相同的电子层结构。X、W的质子数之和等于Y、Z的质子数之和。下列说法错误的是( )
| A.X的离子半径>Y的离子半径 |
| B.Z的氢化物的稳定性<W的氢化物的稳定性 |
| C.Y的氧化物既能与盐酸反应,又能与NaOH溶液反应 |
| D.X2W2、Y2W3两种化合物含有的化学键类型完全相同 |
X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期。下列说法错误的是( )
| A.Y、Z、R 3种元素组成的化合物水溶液一定显碱性 |
| B.原子半径:Z>R>W |
| C.气态氢化物稳定性:HW>H2R |
| D.XW4分子中各原子均满足8电子结构 |
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,下列说法正确的是( )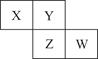
| A.Z元素的原子半径可能比Y元素的小 |
| B.W的原子序数可能是Y的原子序数的2倍 |
| C.W的气态氢化物的稳定性一定比Y的强 |
| D.Z的化学活泼性一定比X强 |
下列说法正确的是( )
A.电子层结构相同的不同离子,其半径随核电荷数增大而减小
B.C、O、S原子半径依次增大,氢化物稳定性逐渐增强
C.ⅠA族元素与ⅦA族元素形成的化合物都为离子化合物
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应的水化物酸性越强