下列说法中正确的是
| A.增大反应物浓度,可逆反应正速率增大;减少反应物浓度,可逆反应逆速率增大 |
| B.粗铜精炼时,电解质液中的c(Cu2+)保持不变 |
| C.纯银在空气中久置变黑发生的是电化学腐蚀 |
| D.阴极电保护法是将被保护的金属与外加电源的负极相连 |
在一定条件下,反应N2+3H2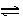 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为()
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为()
| A.V(H2)=0.03mol/(L·min) | B.V(N2)="0.02mol/(L·min)" |
| C.V(NH3)=0.17mol/(L·min) | D.V(NH3)=0.01mol/(L·min) |
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2③Sn(s、灰) Sn(s、白)
Sn(s、白)
△H3=+2.1kJ/mol下列说法正确的是( )
| A.△H1>△H2 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是放热反应 |
| D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏 |
在同温同压下,下列各组热化学方程式中b>a的是()
| A.H2(g)+Cl2(g)=2HCl(g);△H=-a 1/2H2(g)+1/2Cl2(g)=HCl(g);△H=-b |
| B.C(s)+1/2O2(g)="CO" (g);△H=-aC(s)+O2(g)=CO2 (g);△H=-b |
| C.2H2(g)+O2(g)=2H2O(l);△H=-a 2H2(g)+O2(g)=2H2O(g);△H=-b |
| D.S(g)+O2(g)=SO2 (g);△H=-aS(s)+O2(g)=SO2 (g);△H=-b |
25 ℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ·mol-1、285.8 kJ·mol-1、890.3 kJ·mol-1、2 800 kJ·mol-1,则下列热化学方程式正确的是()
A.C(s)+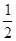 O2(g)====CO(g);ΔH="-393.5" kJ·mol-1 O2(g)====CO(g);ΔH="-393.5" kJ·mol-1 |
| B.2H2(g)+O2(g)====2H2O(g);ΔH="+571.6" kJ·mol-1 |
| C.CH4(g)+2O2(g)====CO2(g)+2H2O(g);ΔH="-890.3" kJ·mol-1 |
D.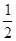 C6H12O6(s)+3O2(g)====3CO2(g)+3H2O(l);ΔH="-1" 400 kJ·mol-1 C6H12O6(s)+3O2(g)====3CO2(g)+3H2O(l);ΔH="-1" 400 kJ·mol-1 |
已知反应:①101 kPa时,2C(s)+O2(g)====2CO(g);ΔH="-221" kJ·mol-1②稀溶液中,H+(aq)+OH-(aq)=H2O(l);ΔH="-57.3" kJ·mol-1。下列结论正确的是()
| A.碳的燃烧热大于110.5 kJ·mol-1 |
| B.①的反应热为221 kJ·mol-1 |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ·mol-1 |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |