下列叙述正确的是( )
| A.元素的单质可由氧化或还原含该元素的化合物来制得 |
| B.得电子越多的氧化剂,其氧化性就越强 |
| C.阳离子只能得到电子被还原,只能做氧化剂 |
| D.含有最高价元素的化合物一定具有强的氧化性 |
综合下图判断,下列叙述不正确的是
| A.Ⅰ、Ⅱ的反应原理均是Zn + Cu2+ = Zn2+ + Cu |
| B.Ⅰ、Ⅱ中均有电子转移,均是把化学能转化为电能利用 |
| C.随着反应的进行,Ⅰ、Ⅱ中CuSO4溶液颜色均渐渐变浅 |
| D.取a中溶液,加足量Ba(NO3)2溶液,过滤后向滤液中加AgNO3溶液,有沉淀产生 |
下列说法正确的是
| A.HClO2 →ClO2+Cl2+H2O(未配平), 1 mol HClO2分解时转移电子的物质的量为1 mol |
| B.标准状况下,14 g CO、C2H4混合气体与11.2 L N2所含有的分子数都是0.5NA |
| C.与金属Cu常温下反应放出气体的溶液可以存在的离子有:Fe2+、Al3+、SO42-、K+ |
D.在燃煤时加入适量石灰石,可减少SO2的排放,其中发生的反应为2CaCO3 +O2+2SO2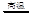 2CaSO3 +2CO2 2CaSO3 +2CO2 |
当身处贴有下列标志的环境时,行为不正确的是
某密闭容器中充入等物质的量的A和B,一定温度下发生反应[A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
| A.30min时降低温度,40min时升高温度 |
| B.反应方程式中的x=1,正反应为吸热反应 |
| C.8min前A的平均反应速率为0.08mol/(L•min) |
| D.30min~40min间该反应使用了催化剂 |
下列有关Fe2(SO4)3溶液的叙述正确的是
| A.该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 |
| B.和KI溶液反应的离子方程式:Fe3++2I-===Fe2++I2 |
| C.1L 0.1mol/L该溶液和足量的Zn充分反应,生成11.2 g Fe |
| D.和Ba(OH)2溶液反应的离子方程式: Fe3++SO42-+Ba2++3OH-===Fe(OH)3↓+BaSO4↓ |