(16分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol·L-1盐酸、0.55 mol·L-1NaOH溶液,实验尚缺少的玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是 。
(3)他们记录的实验数据如下:
| 实验用品 |
溶液温度 |
中和热 |
|||
| t1 |
t2 |
ΔH |
|||
| ① |
50 mL 0.55 mol·L-1 NaOH溶液 |
50 mL 0.5 mol·L-1 HCl溶液 |
20 ℃ |
23.3 ℃ |
|
| ② |
50 mL 0.55 mol·L-1 NaOH溶液 |
50 mL 0.5 mol·L-1 HCl溶液 |
20 ℃ |
23.5 ℃ |
已知:Q=cm(t2-t1),反应后溶液的比热容c为4.18 kJ·℃-1·kg-1,各物质的密度均为1 g·cm-3。
①计算完成上表。
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果 (填“有”或“无”)影响。
(15分)21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
已知:
① Mg(s)+Cl2 (g)=MgCl2 (s) △H=-641 kJ·mol-1
② Cl2(g)+1/2Ti(s)=1/2TiCl4 (l) △H=-385 kJ·mol-1
(1)反应Ⅰ在800~900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式为。
(2)反应Ⅱ的热化学方程式为。
(3)反应Ⅱ中充入气体Ar的原因是。
(4)在800℃~1000℃时电解TiO2也可制得海绵钛,装置如图所示。图中b是电源的极,阴极的电极反应式为。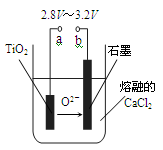
(12分)海水中富含镁,可经过加碱沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,最后电解得到金属镁。
(1)加碱沉淀镁离子时,生成的Mg(OH)2在分散系中处于沉淀溶解平衡,其溶度积常数表达式Ksp=。
(2)MgCl2溶液显酸性,其水解的离子方程式为。
(3)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有。
a.MgO b.Mg(OH)2c.MgCO3d.MgSO4
(4)若在空气中加热MgCl2·6H2O,可生成Mg(OH)Cl或MgO,写出相关的化学方程式之一。
(5)MgCl2·6H2O在干燥的HCl气流中加热可得到无水氯化镁,其原因是。
(6)电解熔融的MgCl2,阳极的电极反应式为:。
(15分)一定条件下,在体积为3 L的密闭容器中化学反应CO(g)+2H2(g)  CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
(1)该反应的平衡常数表达式K=_____________;根据下图,升高温度,K值将____(填“增大”、“减小”或“不变”)。
(2)500 ℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是__________(用nB,tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是____(填字母)。
a.v生成(CH3OH)=v消耗(CO)
b.混合气体的密度不再改变
c.CO、H2、CH3OH的浓度均不再变化
(4)300 ℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是______________(填字母)。
| A.c(H2)减小 | B.正反应速率加快,逆反应速率减慢 |
| C.CH3OH的物质的量增加 | D.重新平衡时c(H2)/c(CH3OH)减小 |
滴定实验是化学学科中重要的定量实验。请回答下列问题:
Ⅰ.酸碱中和滴定——已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250 mL溶液; ②准确量取25.00mL所配溶液于锥形瓶中;
③滴加几滴酚酞溶液;④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
| 滴定序号 |
待测液体积 |
所消耗盐酸标准的体积(mL) |
|
| 滴定前 |
滴定后 |
||
| 1 |
25.00 |
0.50 |
20.60 |
| 2 |
25.00 |
6.00 |
26.00 |
| 3 |
25.00 |
1.10 |
21.00 |
(1)用_____滴定管(填“酸式”或“碱式”)盛装0.10mol/L的盐酸标准液。
(2)试样中NaOH的质量分数为______________________。
(3)若出现下列情况,测定结果偏高的是___________。
a.滴定前用蒸馏水冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管滴至终点对,俯视读数
e.酸式滴定管用蒸馏水洗后,未用标准液润洗
Ⅱ.氧化还原滴定—取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
(4)滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时滴定现象是________________。
Ⅲ.沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
(5)参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是(填选项字母)。
| 难溶物 |
AgCl |
AgBr |
AgCN |
Ag2CrO4 |
AgSCN |
| 颜色 |
白 |
浅黄 |
白 |
砖红 |
白 |
| Ksp |
1.77×10-10 |
5.35×10-13 |
1.21×10-16 |
1.12×10-12 |
1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
(1)有机物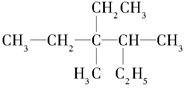 用系统命名法命名:________________________
用系统命名法命名:________________________
(2)写出4甲基2乙基1戊烯的结构简式:________________________
(3)某烃的结构简式是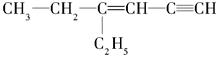 ,分子中饱和碳原子数为_____,可能在同一平面上的碳原子数最多为_________
,分子中饱和碳原子数为_____,可能在同一平面上的碳原子数最多为_________
(4)下列物质中属于同系物的是_________
①CH3CH2Cl②CH2===CHCl③CH3CH2CH2Cl ④CH2ClCH2Cl⑤CH3CH2CH2CH3⑥CH3CH(CH3)2
| A.①② | B.①④ | C.①③ | D.⑤⑥ |
(5)0.1 mol某烷烃燃烧,其燃烧产物全部被碱石灰吸收,碱石灰增39g。该烃的分子式为________;若它的核磁共振氢谱共有3个峰,则该烃可能的结构简式为________。(写出其中一种即可)