常温时,pH值为3的CH3COOH和pH为11的NaOH溶液等体积混合,混合后溶液pH为( )
| A.pH>7 | B.pH< 7 | C.pH=7 | D.无法判断 |
下列叙述正确的是()
| A.标准状况下,11.2 L乙醇中氧原子数为0.5×6.02×1023 |
| B.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023 |
| C.60gSiO2所含Si-O键的数目为2×6.02×1023 |
D.已知AB离子晶体结构如上图所示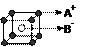 ,则每个A+周围距离最近且等距的B-有8个 ,则每个A+周围距离最近且等距的B-有8个 |
下列实验能达到目的或操作正确的是()
| A.称量NaOH固体时,应先在盘上各放一张干净滤纸,再进行称量 |
| B.配制一定浓度溶液的过程中,容量瓶里有少量晶体未溶解,可在酒精灯上小心加热 |
| C.配制450mL0.5mol/L稀硫酸溶液时,用量筒取22.5mL10mol/L的浓硫酸进行稀释 |
| D.质量分数为w%的氨水与水等体积混合,所得溶液的质量分数小于0.5w% |
下列说法中,正确的一组是()
| A.石墨与金刚石的转化属于物理变化 |
| B.氢键是一种特殊的化学键 |
C. H、 H、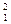 H、 H、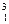 H是氢元素的三种核素,互称为同位素 H是氢元素的三种核素,互称为同位素 |
D.已知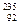 U的质量数为235,则铀元素的相对原子质量可近似为235 U的质量数为235,则铀元素的相对原子质量可近似为235 |
含有1mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是 ()
()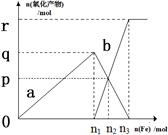
| A.a是Fe(NO3)2 | B.n1 = 0.375 |
| C.p = 0.20 | D.n2 = 0.30 |
在一种酸性溶液中存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推知该 溶液中()
溶液中()
A 一定含有I-,不能确定是否含有Cl- B 一定含有NO3-
C 不含有Fe3+,可能含有NO3-D 一定含有I-、NO3-和Cl-