为了配制NH4+浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入①适量的HCl②适量的NaCl③适量的氨水④适量的NaOH,正确的是( )
| A.①② | B.③ | C.③④ | D.④ |
生活中常常碰到涉及化学知识的某些问题,下列叙述正确的是()
① 人的皮肤在强紫外线的照射下将会失去生理活性
② 用苯酚对食物进行消毒是国家允许的
③ 米酒变酸的过程涉及了氧化反应
④ 棉花和人造丝的主要成分都是纤维素,蚕丝和蜘蛛丝的主要成分都是蛋白质
⑤ 蜂蚁叮咬人的皮肤时将分泌物甲酸注入人体,可在患处涂抹小苏打或稀氨水
| A.①③④⑤ | B.③④⑤ | C.①②④ | D.全部 |
下列三种有机物是某些药物中的有效成分: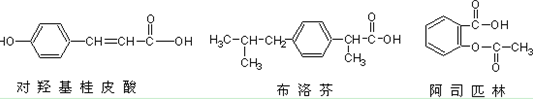
以下说法正确的是()
| A.三种有机物都能与浓溴水发生反应 |
| B.三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 |
| C.将等物质的量的三种物质加入氢氧化钠溶液中,阿司匹林消耗氢氧化钠最多 |
| D.使用FeCl3溶液和稀硫酸不能鉴别出这三种有机物 |
2011年是国际化学年,我国的主题是“化学——我们的生活,我们的未来”。下列有关叙述不正确的是( )
| A.利用可降解的“玉米塑料”生产一次性饭盒,可防止白色污染 |
| B.利用太阳能、潮汐能、风力发电,以获取清洁能源 |
| C.采用纳米二氧化钛光触媒技术将汽车尾气中的NO和CO转化为无害气体 |
| D.常在包装袋内放入生石灰防止月饼等富脂食品氧化变质 |
右图表示4-溴环己烯所发生的4个不同反应。其中,产物官能团种类不会减少的反应是( )
| A.②③ | B.③④ |
| C.①② | D.①④ |
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 2B(g) xC(g)ΔH=-192kJ·mol-1。向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
xC(g)ΔH=-192kJ·mol-1。向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是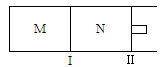
| A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N) |
| B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N) |
| C.若x<3,C的平衡浓度关系为:c(M)>c(N) |
| D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等 |