Na、Cu、O、Si、S、Cl是常见的六种元素。
(l)Na位于元素周期表第___周期第____族;S的基态原子核外有____个未成对电子;Si的基态原子核外电子排布式为___________
(2)用“>”或“<”填空:
| 第一电离能 |
离子半径 |
熔点 |
酸性 |
| Si_____S |
O2-_____Na+ |
NaCl_____Si |
H2SO4____HCl O4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25℃、101kPa下,已知该反应每消耗1molCuCl(s),放热44.4kJ,该反应的热化学方程式是___________________。
(4)ClO2常用子水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目_________________。
(10分)下图表示800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t表示时间。试回答: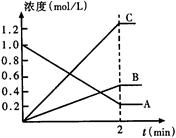
(1)该反应的反应物是。
(2)该反应的化学方程式为。
(3)达到平衡状态的所需时间是2min,A物质的平均反应速率为
(4)其他条件不变,压缩容器容积,平衡______________(填向正或逆方向或不)移动;若正方向吸热,则升高温度,平衡平衡___________(填向正或逆方向或不)移动。
(10分)有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B元素原子L层上的电子数为K层电子数的2倍;C的最高价氧化物对应的水化物与其氢化物反应生成一种铵盐;E与A同主族;元素D的2价阴离子的核外电子排布与氖原子相同;A和E都能与D形成X2Y、X2Y2型化合物。
(1) 写元素符号是: B_____ ; E_______ 。
(2) C的氢化物的电子式_______,其水溶液具有_____性(酸/中/碱)
(3) B的最高价氧化物与E2D2反应的化学方程式为 ____。
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了普遍的重视。
(1)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应: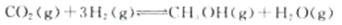
下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。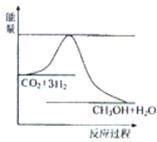
①该反应是(填“吸热”或“放热”)反应。
②反应体系中加入催化剂对反应热是否有影响?(填“是”或“否”),原因是。
(2)若将6mol CO2和8 mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化的曲线如图所示(实线)。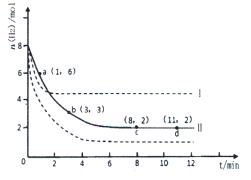
①该条件下反应的平衡常数K=。请在答题卷图中绘出甲醇的物质的量随时间变化曲线。
②仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是,曲线Ⅱ对应的实验条件改变是。
③下列措施中能使H2转化率增大的是。
| A.升高温度 | B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离出来 | D.再充入3mol CO2和4mol H2 |
(3)如将CO2与H2以1:4的体积比混合,在适当的条件下可制得CH4。已知: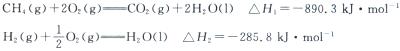
写出CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式。
中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,甲醇燃料电池的工作原理如图所示。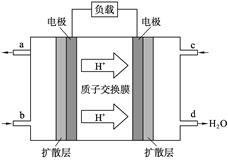
(1)请写出c口通入的物质发生的相应电极反应式。
(2)工作一段时间后,当0.2 mol甲醇完全反应生成CO2时,有NA个电子转移。
(3)以上述电池做电源,用下图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现Al电极附近逐渐变浑浊并有气泡逸出,原因是(用相关的电极反应式表示):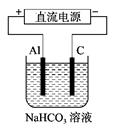
①②Al3++3HCO3- =Al(OH)3↓+3CO2↑
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸 Ka= 1.75×10-5
碳酸 Ka1= 4.30×10-7 Ka2 = 5.61×10-11
亚硫酸 Ka1= 1.54×10-2 Ka2 = 1.02×10-7
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = ;
碳酸的第一步电离比第二步电离(填“容易” 或 “困难”)。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:>>
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是(填序号)
| A.c(CH3COO-) | B.c(H+) | C.醋酸的电离平衡常数 | D.醋酸的电离度 |