有Fe2+、NO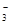 、Fe3+、NH
、Fe3+、NH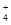 、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是
、H+和H2O六种粒子,分别属于同一氧化还原反应中的反应物和生成物,下列叙述错误的是
| A.氧化剂与还原剂的物质的量之比为1:8 |
B.若有1molNO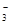 发生氧化反应,则转移8mol电子 发生氧化反应,则转移8mol电子 |
| C.该过程说明Fe(NO3)2溶液不宜加酸酸化 |
| D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ |
下列说法错误的是( )
| A.1.5g CH3+中含有的电子数为0.8NA | B.Cu元素在元素周期表的ds区 |
| C.s轨道呈圆形,p轨道呈哑铃形 | D.DNA中的碱基互补配对是通过氢键来实现的 |
下列叙述中正确的是()
| A.HClO4、H2SO4、H3PO4的酸性由强到弱 | B.HF、HCl、HBr、Hl的稳定性依次增强 |
| C.金属的熔点和沸点都很高 | D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列物质的熔、沸点高低顺序正确的是()
| A.金刚石>晶体硅>二氧化硅>碳化硅 | B.CI4>CBr4>CCl4>CF4 |
| C.K2O>Na2O>O2>N2 | D.干冰 >二氧化硅>氯化钠>钠 |
已知某+2价离子的电子排布式为1s22s22p63s23p63d9,该元素在周期表中所属的族是()
| A.IB | B.IIA | C.IIB | D.VIII |
下列各组数值是相应元素的原子序数,其中所表示的原子能以离子键结合成稳定化合物的是
| A.1与6 | B.2与8 | C.9与11 | D.8与14 |