已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是( )
A. 元素A、B组成的化合物常温下一定呈气态
B.元素C、D的最高价氧化对应的水化物之间不能发生反应
C. 化合物AE与CE含有相同类型的化学键
D. 工业上常用电解法制备元素C、D的单质
下列各种烃与氢气完全加成后,能生成2,3,3-三甲基戊烷的是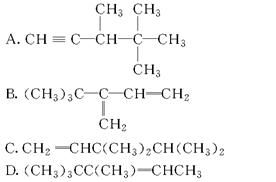
下列化学用语正确的是
A.乙酸根离子的结构式: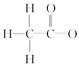 |
B.CO2分子的球棍模型: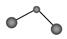 |
| C.3甲基1丁烯的结构简式:(CH3)2CHCH=CH2 |
D.醛基的电子式为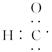 |
【改编】下列有关有机化合物的说法正确的是
| A.用水可以区分乙酸乙酯和苯 |
| B.有机物分子中都存在碳碳单键 |
| C.聚乙烯不可以使溴水褪色 |
| D.乙醇、油脂、淀粉是人们必需的营养物 |
下列对有机化合物的分类结果正确的是
| A.乙烯CH2===CH2、苯、环己烷都属于脂肪烃 |
B.苯、环戊烷 、环己烷同属于芳香烃 、环己烷同属于芳香烃 |
| C.乙烯CH2===CH2、乙炔CHCH同属于烯烃 |
D. 同属于环烷烃 同属于环烷烃 |
【改编】一种兴奋剂X的结构如图所示.下列说法的错误是
| A.一定条件下,1mol X与足量NaOH溶液反应,最多可消耗5mol NaOH |
| B.1mol X与足量浓溴水反应,最多消耗4mol Br2 |
| C.X遇FeCl3溶液显紫色 |
| D.分子中不含氧的官能团有3种 |