实验题:
(1)写出下图中序号①~③仪器的名称: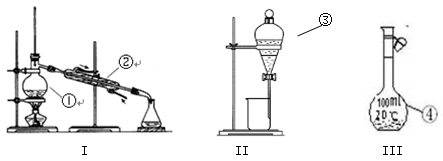 ① ; ② ; ③ 。
① ; ② ; ③ 。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填仪器序号)
(3)下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。
可供选用的仪器有:①胶头滴管 ②烧瓶 ③烧杯 ④玻璃棒 ⑤药匙 ⑥量筒 ⑦托盘天平。
请回答下列问题:
①.该硫酸的物质的量浓度为 mol·L-1。
②.配制稀硫酸时,还缺少的仪器有 (写仪器名称)。
③.经计算,配制480mL1mol· L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为
mL。
④.对所配制的稀硫酸进行测定,发现其浓度小于1 mol/L,配制过程中下列各项操作可能引起该误差的原因有 。(填字母)
| A.定容时,俯视容量瓶刻度线进行定容 |
| B.将稀释后的硫酸未经冷却直接转移至容量瓶中 |
| C.转移溶液时,不慎将少量溶液洒到容量瓶外面 |
| D.所用容量瓶经蒸馏水洗涤后未干燥,有少量残留蒸馏水 |
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,再滴水至刻度线处
按下图装置进行实验:
(1)实验一段时间后,可观察到锥形瓶口上方有白烟生成,请将可能观察到的其他现象补齐:;
有关化学方程式是
(2)由于气温的原因,上述实验一段时间后现象不太明显,需向锥形瓶内加入下列哪种物质才能看到明显现象(填代号)。
| A.氢氧化钠固体 | B.生石灰 | C.浓硫酸 | D.氯化铵固体 |
根据从草木灰中提取钾盐的实验,填写下列空白:
(1)此实验操作顺序如下:①称量样品,②溶解、沉淀,③,④,⑤冷却结晶。
(2)用托盘天平(指针向上的)称量样品,若指针偏右边,则表示。
| A.左盘重,样品轻 | B.左盘轻,砝码重 | C.右盘重,砝码轻 | D.右盘轻,样品重 |
(3)在进行第③步操作时,有时可能要重复进行,这是由于。
(4)在进行第④步操作时,有时要有玻璃棒不断小心地搅动液体,目的是防止。
(5)所得产物中主要钾盐有、、(填化学式)。
下面是实验室制取肥皂的实验步骤:①在蒸发皿中加入8mL植物油、8mL乙醇和4mLNaOH溶液;②把盛有混合物的蒸发皿放在冷水中冷却;③在不断搅拌下,给蒸发皿中的液体微微加热,直到混合物变稠;④向混合物中加入20mL热蒸馏水,再放在冷水中冷却;⑤加入25mLNaCl饱和溶液,充分搅拌;⑥继续加热,直到把一滴混合物放到水中时,在液体表面不再形成液滴为止;⑦用纱布滤出固体物质,弃去废液。把固体物质挤干,并压成条状,晾干,即制得肥皂。
(1)上述实验的正确操作步骤是。
(2)加入乙醇的作用是什么?
(3)加入饱和NaCl溶液的作用是什么?
(4)如何检验皂化反应是否完全?。
(5)写出上述制取反应的化学方程式。
(18分)50 mL0.5mol/L盐酸跟50mL0.55mol/L氢氧化钠溶液在下图装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题。
(1)实验目的:
(2)实验用品:烧杯(500 mL和100 mL各1只)、温度计、塑料泡沫板(或硬纸板)、泡沫塑料或纸条、(填写所缺的实验仪器);0.50mol/L盐酸、0.55mol/L NaOH溶液
(3)实验步骤:(略)
(4)问题与结论:
①完整地做一次这样的实验,需测定次温度。
②大小烧杯间填满碎纸条、大烧杯上加盖硬纸板的作用是。
③该实验中NaOH溶液的浓度大于盐酸浓度的作用是。
④大烧杯上如不盖硬纸板,对求得中和热的数值有何影响:理由:
⑤改用60 mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液进行反应,与上述实验相比,所放热量是否相等:所求中和热数值是否相等:。
.选择下列实验方法提纯或分离下列物质,将分离方法的序号填入表格中。
| A.萃取 | B.升华 | C.蒸发 | D.分液 E.蒸馏 F.过滤 |
| 分离或提纯的物质 |
分离方法 |
| 分离BaSO4和BaCl2溶液 |
|
| 分离食盐和碘 |
|
| 分离花生油和水 |
|
| 从碘水中提取碘单质 |
|
| 用自来水制取蒸馏水 |
|
| 从溶液中获得硫酸钠晶体 |