下图是初中化学中常见物质间的转化关系。其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体且1 mol E中含有 10 mol电子。乙和丁为黑色固体,将它们混和加热后发现固体由黑色变为红色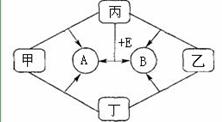
(1)写出化学式:甲_________ ;乙________;丙_______;
(2)丁的摩尔质量为_____ ____ 。
(3)写出丙和E反应生成A和B的化学方程式: ____________________________
(4)有学生将乙和丁混和加热后收集到标准状况下气体8.96 L ,测得该气体对氢气的相对密度为16, 若将气体通入足量的澄清石灰水中,得到白色沉淀物 g
(1)等物质的量的CH4和NH3,其质量比为________,分子个数比为______,原子个数比为_______,氢原子个数比为________。
(2)2 mol CO2的质量为________g,含分子数约为______个,在标准状况下所占有的体积约为______L,含氧原子的物质的量为______mol。
(3)0.3 mol的氧气和0.2 mol的臭氧O3,它们的质量之比是________,分子数之比是________,原子数之比是________,它们的体积比(同温、同压)是________。
(4)质量为16g的CH4其物质的量为________,分子个数为________,原子个数为________,氢原子个数为________。
将6.5 g锌投入200 mL某浓度的稀盐酸中,锌和稀盐酸恰好完全反应。求:
(1)6.5g锌的物质的量为 ;
(2)所用稀盐酸中HCl的物质的量浓度为 ;
(3)反应中生成的H2在标准状况下的体积 ;
(4)向反应后的溶液中加水至500 mL,求此时氯化锌的物质的量浓度 。
现有m g某气体,它由双原子分子构成,它的摩尔质量为M g / mol。若阿伏加德罗常数的值用NA表示,则:(注意填写单位)
(1)该气体的物质的量为______________。
(2)该气体所含原子总数为________________。
(3)该气体在标准状况下的体积为_______________。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为___。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为 。
用于分离或提纯物质的方法有:A蒸馏(分馏) B盐析C过滤 D重结晶 E升华 F渗析 G加热分解。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(把选用的方法的标号填入括号内)
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒()
(2)除去Fe(OH)3胶体中混有的Cl-离子()
(3)除去乙醇中的少量水()
(4)除去氧化钙中的碳酸钙()
(5)除去固体碘中混有的砂子()
17gNH3共有 mol氢原子,0.1molH2S共有约 个原子,同温同压下,同体积的NH3和H2S气体的质量比为 ;同温同压下,同质量的NH3和H2S气体的体积比为