现有m g某气体,它由双原子分子构成,它的摩尔质量为M g / mol。若阿伏加德罗常数的值用NA表示,则:(注意填写单位)
(1)该气体的物质的量为______________。
(2)该气体所含原子总数为________________。
(3)该气体在标准状况下的体积为_______________。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为_ __。
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为 。
某化学反应的反应物和产物如下:Al+NaNO3+H2O→Al(OH)3+N2+NaAlO2
(1)该反应的氧化剂是_____________。
(2)该反应的氧化产物是______________。
(3)反应过程中转移5 mol e-,生成标准状况下N2的体积__________ L。
(4)配平该反应的化学方程式:___Al+____NaNO3+___H2O=______Al(OH)3+____N2+___NaAlO2。
下图中的每一方格表示有关的一种反应物或生成物,其中甲、乙、丙、丁为常见单质,其余均为化合物,A是一种常见的液态化合物,B是具有磁性的氧化物,D和丁既能和酸反应又能和碱反应,乙在丙中燃烧产生苍白色火焰,它们的转化关系如下:(有些反应的条件和部分产物未注明)
(1)上述反应中属于氧化还原反应的是(填写序号);
(2)写出下列物质化学式:B,D,F;
(3)写出反应的化学方程式:A+甲;
(4)H在空气中很容易被氧化成I,该过程的实验现象是;将足量的CO2通入E溶液中,离子方程式是。
钠的化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)碳酸氢钠俗称,水溶液呈性。碳酸氢钠粉末可用于治疗胃酸(0.2%-0.4%的盐酸)过多,反应的离子方程式是;
(2)除去NaHCO3溶液中少量的Na2CO3溶液,(填“能”或“不能”)用足量的澄清石灰水,原因是_______________用离子方程式表示);等质量的碳酸钠和碳酸氢钠分别与足量稀盐酸反应产生气体的物质的量之比;
(3)过氧化钠可用于呼吸面具或潜水艇中氧气的来源,写出化学反应方程式,并用双线桥法标电子转移的方向和数目;若有5. 6L水蒸气通过一 定质量的过氧化钠粉末后,气体体积减小到4.48 L,则气体的成分是,气体的总质量是。(气体体积已折算成标准状况)
信息时代产生的大量电子垃圾对环境构成严重威胁。某研究性学习小组将一批废弃的线路板简单处理后,得到含Cu、Fe及少量Au、Pt等金属的混合物,并用如下流程制备胆矾晶体(CuSO4•5H2O):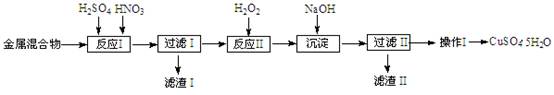
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 |
Fe3+ |
Fe2+ |
Cu2+ |
| 开始沉淀 |
1.5 |
6.4 |
4.2 |
| 完全沉淀 |
3.2 |
8.9 |
6.7 |
(1)滤渣Ⅰ的主要成份是(写化学式)______。
(2)反应Ⅱ中加入H2O2的作用是______。
(3)沉淀过程中发生反应的离子方程式有______、______。
(4)操作Ⅰ的步骤是______、______、过滤、洗涤、干燥。
(5)测定胆矾晶体纯度的实验步骤如下:
a. 准确称取3.125g胆矾晶体样品配成100mL溶液;
b. 取10.00 mL溶液于带塞锥形瓶中,加适量水稀释,加入过量KI固体,发生反应:
2Cu2+ +4Iˉ=2CuI↓ + I2
c. 继续向上述混合物中,逐滴加入0.1000 mol·L-1Na2S2O3溶液至恰好完全反应,共消耗12. 00mL Na2S2O3溶液:I2+2S2O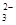 = 2Iˉ+S4O
= 2Iˉ+S4O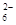
求样品中胆矾晶体的质量分数(写出计算过程)。
在下图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体。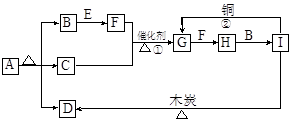
完成下列问题:
(1)写出A的化学式。
(2)组成F的元素在周期表中位于周期族。
(3)B的电子式是。
(4)反应①的化学方程式:。
(5)反应②的离子方程式:。