电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代。处理有氰电镀的废水一般采用氧化法,常用的氧化剂有氯气、二氧化氯、次氯酸盐双氧水等。
(1)工业上常用双氧水处理含CN-离子浓度较低的废水,流程如下:
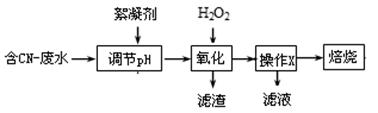
操作X的名称为 。滤液中常含有H2O2,排放前需除去,写出除去H2O2的方法
(2)实验室中可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成OCN-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol·L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。
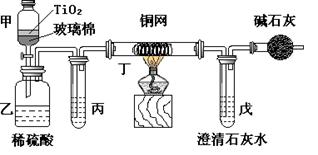
回答下列问题:
①乙中反应的离子方程式为 。丁在实验中的作用是 。
②乙中生成的气体除N2和CO2外,还有副产物HCl及Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是 (填字母)
| A.饱和食盐水 | B.饱和NaHCO3溶液 | C.浓NaOH溶液 | D.浓硫酸 |
③若该测得值与实际处理的百分率相比偏低,请简要说明可能的原因 。请提出一个能提高准确度的建议(具体操作) 。
④处理后的溶液,主要含有HClO、Na+、H+、Cl-等,请设计实验证明溶液中含有HClO和H+的实验方案:
阅读下列材料后,完成相应问题。
一个体重50 kg的健康人,含铁2 g。这2 g铁在人体中不以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。二价铁离子(亚铁离子)易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可以使食物中的铁离子(三价铁离子)变成亚铁离子,以利于铁的吸收。
(1)人体中经常进行Fe2+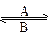 Fe3+的转化,A中Fe2+被__________,B中Fe3+作__________剂。
Fe3+的转化,A中Fe2+被__________,B中Fe3+作__________剂。
(2)从“服用维生素C,可以使食物中的铁离子变成亚铁离子”这句话分析出维生素C在这一反应中作__________剂,具有__________性
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。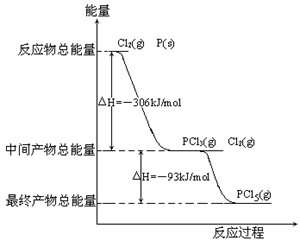
根据上图回答下列问题:
(1)P和Cl2反应生成PCl5(g)的热化学方程式
(2)PCl5(g)分解成PCl3(g)和Cl2的热化学方程式
上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入1.60molPCl5,反应达到平衡时PCl5有1.20mol,其分解率α1,若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,则α2_______α1(填“大于”、“小于”或“等于”)。
(3)工业上制备PCl5通常分两步进行,先将P和Cl2反应生成中间产物PCl3,然后降温,再和Cl2反应生成PCl5。原因是_________________________________。
(4)P和Cl2分两步反应生成1molPCl5的焓变为△H3,P和Cl2一步反应生成1molPCl5的焓变为△H4,则△H4______△H3(填“大于”、“小于”或“等于”)。
(5)以红磷P(s)和Cl2(g)制备PCl5,为提高Cl2(g)的转化率可采用的措施是:
(任填两种措施)
(6分)可逆反应①X(g)+2Y(g) 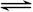 2Z(g) 、②2M(g)
2Z(g) 、②2M(g) 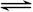 N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
N(g)+P(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示: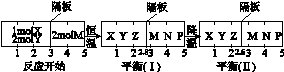
则X(g)+2Y(g) 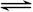 2Z(g)正反应为反应(填“放热”或“吸热”)达到平衡(Ⅰ)时X的转化率为(保留小数点后两位数字,下同);假设平衡(Ⅰ)时左边容器(X、Y、Z的体系)的体积为2L,求此温度下的化学平衡常数
2Z(g)正反应为反应(填“放热”或“吸热”)达到平衡(Ⅰ)时X的转化率为(保留小数点后两位数字,下同);假设平衡(Ⅰ)时左边容器(X、Y、Z的体系)的体积为2L,求此温度下的化学平衡常数
下图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。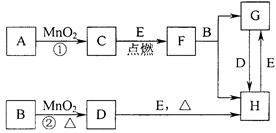
(1)写出有关物质的名称或化学式:F,H。
若反应①是在加热条件下进行,则A是;若反应①是在常温条件下进行,则A是。
(2)写出B与MnO2共热获得D的离子方程式 。
。
(3 )B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4
)B的稀溶液与AgNO3溶液混合可形成沉淀AgX,此沉淀的Ksp(AgX) =1.8×10-10。将等体积的B稀溶液与AgNO3溶液混合,若B的浓度为2×10—4 mo1/L
mo1/L  ,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象,沉淀能够发生转化的原因是。
,则生成沉淀所需AgNO3溶液的最小浓度为________。若向AgX悬浊液中滴加KI溶液,观察到的现象,沉淀能够发生转化的原因是。
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)Z原子的结构示意图为
(2)用电子式表示X与W组成的化合物的形成过程
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为 。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。写出加热条件下A与NaOH溶液反应的离子方程式 。
。
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式 。
。