一辆载有近30吨苯酚的槽罐车途经某市时发生侧翻,约有10吨的苯酚泄漏,空气中弥漫着浓烈的酸臭气味,对当地居民生活造成很大威胁,苯酚是一种有毒的物质,对皮肤、黏膜有强烈的腐蚀作用。
(1)苯酚的化学式为(C6H6O)属于________(填“有机物”或“无机物”)。
(2)现场救护人员应佩戴呼吸器,穿好防化服的原因是__________________________________。
(3)你认为下列对事故的处理方法合理的是( )
①用水进行冲洗或用泥土填埋苯酚
②挖隔离沟、铺薄膜防止扩散并回收泄漏的苯酚
③随时监测附近水源、土壤中的苯酚含量
(4)用木屑吸附残余的苯酚,然后燃烧处理,写出苯酚完全燃烧的化学方程式______________。
色香味俱佳、口感好的食品深受人们的喜爱。为了提高食品的质量,在生产过程中往往会加入一些能改变食品某些性质的物质(即食品添加剂)。
(1)味精是常用的一种鲜味剂,其有效成分是谷氨酸钠,它的结构简式是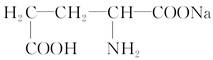 ,该物质分子中所含的官能团有________和________(填写名称)。
,该物质分子中所含的官能团有________和________(填写名称)。
(2)碳酸氢钠是常见的疏松剂,主要是因为它在加热条件下产生了气体,使食品变得疏松。试写出碳酸氢钠受热分解的化学方程式:__________________________________。
据中央电视台新闻报道,某知名品牌保健食品补钙剂经检测,H2O2含量超标,试回答下列问题.
(1)该品牌保健食品属于________的保健食品。
A.强化营养人群
B.特殊人群
C.健康异常人群
(2)试推测该保健食品中钙以________的方式存在。
A.钙单质B.Ca(OH)2 C.CaCO3D.乳酸钙
(3)试写出超标的H2O2的电子式________。
(4)某成年女子,经化验知缺铁,如果该女子也使用补铁保健食品,能否与该品牌保健食品同时食用________,如果不能,试用化学方程式表示其原因__________________________。
某种甜味剂A的甜度是蔗糖的200倍,由于它热值低、口感好、副作用小,已在90多个国家广泛使用。A的结构简式为: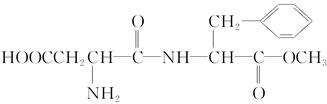
已知:①在一定条件下,羧酸酯或羧酸与含—NH2的化合物反应可以生成酰胺,如: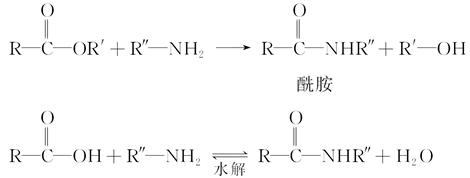
②酯比酰胺容易水解。请填写下列空白:
(1)在稀酸条件下加热,化合物A首先生成的水解产物是________和________。
(2)在较浓酸和长时间加热条件下,化合物A可以水解生成________、________和________。
(3)化合物A分子内的官能团之间也可以发生反应,再生成一个酰胺键,产物是甲醇和________________。(填写结构简式,该分子中除苯环以外,还含有一个六原子组成的环)。
某有机物含碳、氢、氧、氮四种元素。如图是该有机物的球棍模型(其中黑点表示原子,短线表示原子之间的共价键),则该有机物的化学式为________________________。
写出该有机物的一种同分异构体,它的分子中含有两个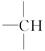 ,且是天然蛋白质水解的最终产物之一,则该同分异构体的结构简式为_____________________________________。
,且是天然蛋白质水解的最终产物之一,则该同分异构体的结构简式为_____________________________________。
下面是关于药物华素片(西地碘片)使用说明书中的部分内容:
(1)根据上述说明和所学化学知识回答。
①华素片中含有的活性成分是________(写分子式);
②请推断华素片________(“是”或“不是”)白色。
(2)某学生为验证华素片中确实含有上述成分,设计实验如下,请填写空格。
①取一粒药片放入研钵中研碎,再将药粉装入试管并加入约2 mL蒸馏水。
向该试管中再加入约2 mL________(填选项字母),并用力振荡。
| A.酒精 | B.热裂汽油 |
| C.四氯化碳 | D.甘油 |
②描述加入该液体后可能观察到的现象______________________________。
③选用该液体做实验的原因是____________________________________________。
(3)还可以用另一种试剂验证华素片中的成分,试剂是________,现象是____________________________________。