设NA为阿伏加德罗常数的值,下列说法正确的是
| A.20 g氖气中所含的原子数目为NA |
| B.25℃时,pH=12的NaHCO3溶液中含有OH-的数目为0.01NA |
| C.含NA个阴离子的Na2O2溶于水形成1 L溶液,其物质的量浓度为1 mol·L-1 |
| D.常温常压下,6.4 g Cu与40 mL 10 mol·L-1浓HNO3作用,产生NO2分子的数目为0.2NA |
下列说法正确的是
| A.用硫酸铁作净水剂 | B.自来水厂用盐酸进行消毒杀菌 |
| C.用苏打治疗胃酸过多 | D.用铝制餐具长时间存放咸的食物 |
下列各组离子能在溶液中大量共存的是
| A.Mg2+、H+、C1-、OH- | B.K+、H+、NO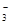 、CO 、CO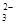 |
C.Na+、OH-、Cl-、SO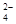 |
D.Na+、Ba2+、CO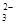 、NO 、NO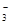 |
不能用来检验新制氯水和久置氯水的试剂是
| A.石蕊试液 | B.品红溶液 | C.FeCl2溶液 | D.AgNO3溶液 |
下列关于金属的说法不正确的是
| A.在自然界都以化合态存在 |
| B.易导电、易导热、有延展性 |
| C.金属元素原子的最外层电子数较少,易失去 |
| D.多数金属能被Cl2、S氧化,生成相应的氯化物或硫化物 |
下列转化不能通过一步反应实现的是
| A.Na→Na2O2 | B.Al(OH)3→Al2O3 |
| C.Fe2O3→Fe(OH)3 | D.Fe(OH)2→Fe(OH)3 |