某兴趣小组采用HgSO4作催化剂,使乙炔水化为乙醛(在75℃左右)。但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种。现选用块状电石、浓H2SO4、水、NaOH溶液、HgO粉末五种物质制乙醛,装置图如下所示,回答下列问题: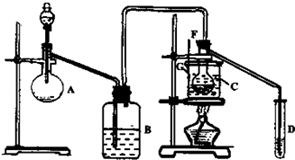
(1)实验开始时,仪器A中盛放电石,B中应装入_______,其作用是_________ 。
(2)仪器D中盛放水,其作用是__________________________________________ 。
(3)蒸馏烧瓶F中应加入HgO和另外两种试剂,若将三者分别直接加入,请按加入的先后顺序写出包括HgO在内的各种试剂的名称_______________________ 。
(4)所选用温度计G的量程表示正确的是________ 。
| A.0℃~50℃ | B.0℃~100℃ | C.0℃~200℃ | D.50℃~100℃ |
(5)检验乙醛已制出的操作、现象是______________________________________ 。
(14分)二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸,易与碱液反应生成盐和水。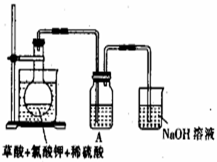
(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为

①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间。控制温度的目的是,图示装置中缺少的一种必须的玻璃仪器是
②装置A用于溶解产生的二氧化氯气体,其中最好盛放(填字母)。
| A.20mL 60℃的温水 | B.100mL冰水 |
| C.100mL饱和食盐水 | D.100mL沸水 |
③在烧瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(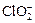 )。饮用水中ClO2、
)。饮用水中ClO2、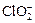 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点。
①步骤1中若要量取20.00mL水样,则应选用的仪器是
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为: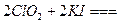
 ,则步骤4中加入的指示剂为,滴定达到终点时溶液的颜色变化为
,则步骤4中加入的指示剂为,滴定达到终点时溶液的颜色变化为
③步骤5的目的是使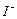 将溶液中的
将溶液中的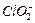 还原为
还原为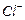 以测定其含量,该反应的离子方程式为:
以测定其含量,该反应的离子方程式为:
④若饮用水中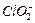 的含量超标,可向其中加入适量的
的含量超标,可向其中加入适量的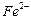 将
将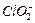 还原为
还原为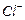 ,则该反应的氧化产物为(填化学式)
,则该反应的氧化产物为(填化学式)
通过实验事实的验证与讨论,认识苯的结构式。提出问题:苯分子结构是碳碳单双键交替的环状结构吗?
(1)提出假设:从苯的分子式看,C6H6具有不饱和性,从苯的凯库勒结构式看,分子中 含有碳碳双键,所以苯一定能使褪色。
含有碳碳双键,所以苯一定能使褪色。
(2)实验验证:
①苯不能使褪色;
②经科学测定,苯分子里6 个碳原子之间的健;6个碳原子和6个氢原子都在同一上。
个碳原子之间的健;6个碳原子和6个氢原子都在同一上。
(3)结论:苯的凯库勒结构式中的双键跟烯烃双键;苯的性质没有表现出不饱和性,结构稳定,说明苯分子 一般的碳碳单、双交替的环状结构。
一般的碳碳单、双交替的环状结构。
为验证木炭与浓硫酸反应生成物中有二氧化硫和二氧化碳,选用下图仪器(含所盛物质),组装成套实验装置,试回答下列问题。
(1)在实验进行中,按气流方向从左到右顺序,A、B、C、D各装置的连接应该(用字母符号)是:。
(2)试管B、C、D中各有什么现象,才能表示已检出二氧化碳、二氧化硫?
B中为。 C中为D中为。
(3)写出A装置中反应化学方程式: 。
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用右图所示的装置制取乙酸乙酯。回答下列问题: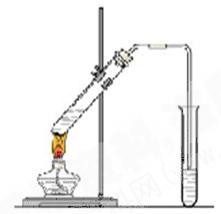
(1)写出制取乙酸乙酯的化学反应方程式。
(2)浓硫酸的作用是。
(3)饱和碳酸钠溶液的主要作用是
。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
防止 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 。
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:
苯甲醛易被空气氧化;苯甲醇的沸点为205.3℃;苯甲酸的熔点121.7℃,沸点249℃,溶解度0.34g(常温);乙醚的沸点34.8℃,难溶于水。
制备苯甲醇和苯甲酸的主要过程如下:
(1)混合苯甲醛、氢氧化钾和水应选用的仪器是 (填序号)。
(填序号)。
A.带胶塞的锥形瓶 B.烧杯
C.容量瓶
(2)操作I的名称是 。
。
(3)操作II的名称是,产品甲的成分是。
(4)操作III的名称是,产品乙是。
(5)在使用下图所示的仪器的操作中,温度计水银球x的放置位置为(填图标a、b、c、d)。控制蒸气的温度为。