A+B→X+Y+ H2O(为配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4.请回答:
(1)若Y是黄绿色气体,则Y的电子式是 ,该反应的化学方程式是 .
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 .
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中.
①A元素在周期表中的位置是______(填所在周期和族);Y的化学式是______.
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是______ mol.
(4)若A、B、X、Y均为化合物.A溶于水电离出的阳离子和水作用的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色.则向A中逐滴加入B的离子方程式 .
(1),
(2),
(3)NH3·H2O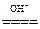 NH3↑+H2O,
NH3↑+H2O,
(4)。
(1)少量Cl2通入FeI2(aq)中,反应的离子方程式是;
(2)过量Cl2通入FeI2(aq)中,反应的离子方程式是;
(3)将1.2 mol Cl2通入含有FeI2 1.0 mol的水溶液中:。
(2)在以上中性溶液中,继续滴加Ba(OH)2(aq),请写出此步反应的离子方程式_______________。
(1)将NaAlO2(aq)和AlCl3(aq)混合:(水解相互促进,反应进行到底,下同);
(2)将10.00 mL 0.10 mol·L-1的NaHCO3(aq)与5.00 mL 0.10 mol·L-1的KAl(SO4)3(aq)混合:。
(1)__________________________________;
(2)__________________________________;
(3)__________________________________(可不写满,也可补充)。