某化学兴趣小组在课外活动中,对某一份溶液成分(已知不含其他还原性离子)进行了检测,其中三次检测结果如下表所示
| 检测序号 |
溶液中检测出的离子组合 |
| 第一次 |
KCl、K2SO4、Na2CO3、NaCl |
| 第二次 |
KCl、AlCl3、Na2SO4、K2CO3 |
| 第三次 |
Na2SO4、KCl、K2CO3、NaCl |
则下列说法合理的是
A.三次检测结果都正确
B.该溶液中的阳离子无法判断
C.为了检验SO42-,应先加过量稀硝酸后再滴加Ba(NO3)2,观察是否有沉淀现象
D.为了确定是否存在CO32-,可以向其中滴加CaCl2溶液,观察是否有沉淀现象
化学与人类的衣食住行以及能源、信息、材料、环境、医药、资源密切相关。下列说法不正确的是()
| A.用食醋可除去热水壶内壁的水垢 |
| B.钢铁制品生锈主要是电化学腐蚀所致 |
| C.酸雨是pH小于7的雨水 |
| D.服用铬含量超标的药用胶囊会对人体健康造成危害 |
下列化学实验事实及其结论都正确的是()
| 选项 |
实验事实 |
结论 |
| A |
将SO2通入含HClO的溶液中生成H2SO4 |
HClO的酸性比H2SO4强 |
| B |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面氧化铝熔点高于铝 |
| C |
SiO2可以和NaOH溶液及HF溶液反应 |
SiO2属于两性氧化物 |
| D |
将SO2通入溴水中,溴水褪色 |
SO2具有漂白性 |
物质间纷繁复杂的转化关系是化学的魅力所在,下列选项中物质的转化在一定条件下不能实现的是()
| 选项 |
转化关系 |
| A |
 |
| B |
 |
| C |
 |
| D |
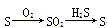 |
下列实验的现象与对应结论均不正确的是()
| 选项 |
操作 |
现象 |
结论 |
| A |
将浓硫酸滴到蔗糖表面 |
固体变黑膨胀 |
浓硫酸有脱水性和强氧化性 |
| B |
常温下将Al片放入浓硝酸中 |
无明显现象 |
Al与浓硝酸发生钝化 |
| C |
将一小块Na放入无水乙醇中 |
产生气泡 |
Na能置换出醇羟基中的氢 |
| D |
将水蒸气通过灼热的铁粉 |
粉末变红 |
铁与水在高温下发生反应 |
SiO2是一种化工原料,可以制备一系列物质。下列说法正确的是()
| A.图中所有反应都不属于氧化还原反应 |
| B.硅酸盐的化学性质稳定,常用于制造光导纤维 |
| C.可用盐酸除去石英砂(主要成分为SiO2)中少量的碳酸钙 |
| D.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高 |